化学势与平衡驱动力
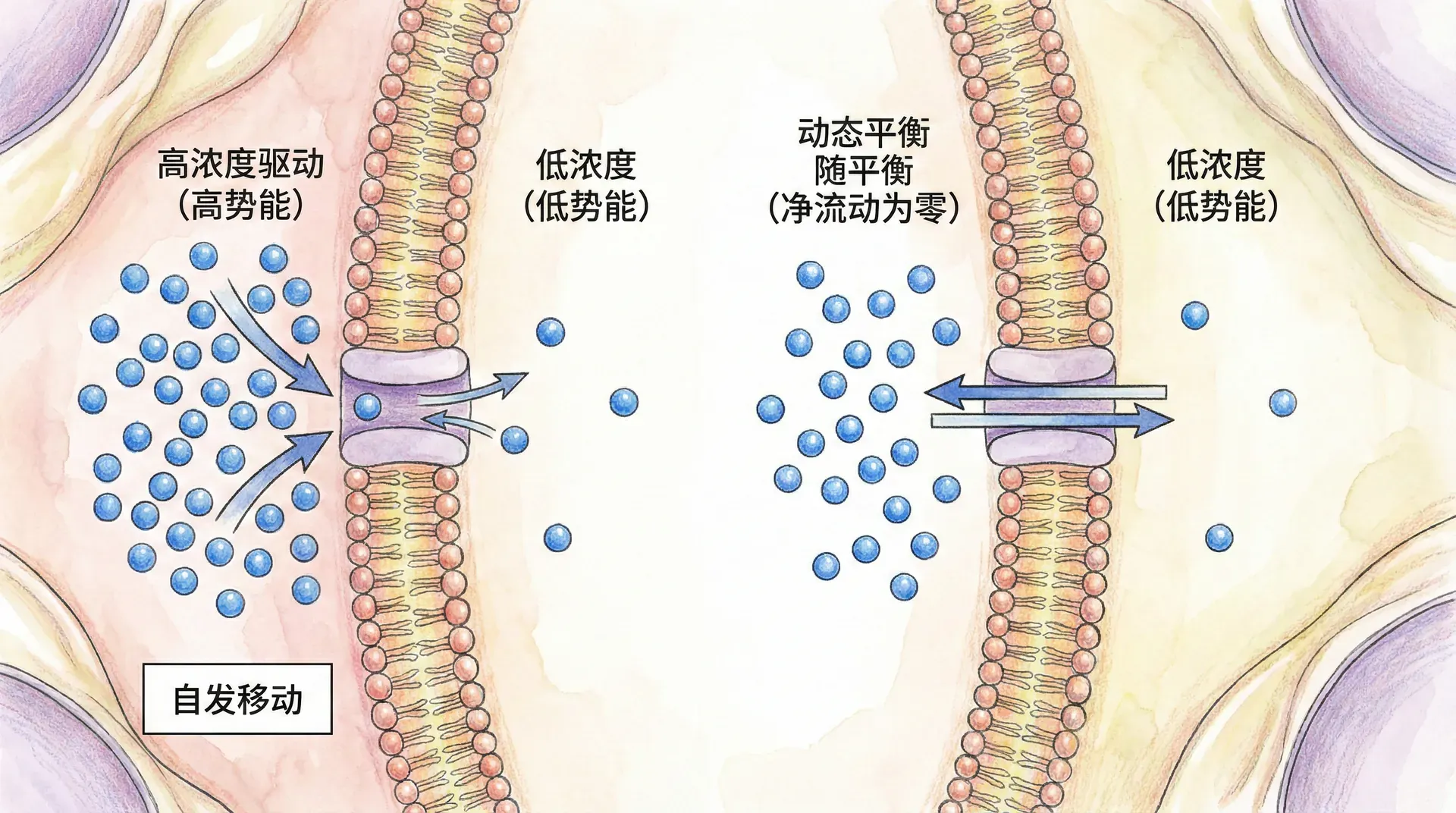
化学势可以被形象地理解为分子世界中的“水流”或“能量高差”,它决定了物质究竟会从哪儿流向哪儿。就如同日常生活中水总是从高处流向低处一样,在分子层面,物质也始终倾向于自发地从化学势高的地方迁移到化学势低的地方,这种“流动”贯穿着各种自然和生命过程。虽然“化学势”这个名词听起来有些抽象,实际上它无时无刻不在主导着我们体内外的各种生化反应。
例如,从血液中氧气如何被携带到全身各处组织、到细胞中蛋白质和其他大分子的合成,再到神经元之间复杂的信号传递——这些维持生命的关键活动背后,往往都是化学势在做功。化学势的“高低”就像为分子的运动和反应设定了方向,使得生命体系中能量转化和物质流动得以高效而有序地进行。进一步来说,正是由于不同分子、离子、乃至能量载体之间存在化学势差,细胞才有动力吸收营养、排除废物,器官之间才能协同工作,整个生命活动得以持续和协调。因此,化学势不仅仅是一个能量高低的抽象数字,更是生物世界中维系平衡、驱动变化的核心力量。
化学势
化学势的本质含义
化学势可以理解为每摩尔物质所具有的自由能,它描述了在恒定温度和压力下,系统中该组分摩尔数微小变化时自由能的增量。换句话说,化学势反映了物质发生转移或反应的“动因”有多大。虽然这个定义听起来带有数理哲学的色彩,其实我们可以用身边的例子来形象理解。
比方说,中国传统的梯田层层叠叠,水总是自上而下流动,最终在每一层梯田间形成平衡。在分子世界中,化学势就相当于“分子的高度”,分子总是倾向于从化学势高的区域自发移动到低的区域,从而驱动扩散、渗透、反应等各种过程。这一过程会持续到体系内各处的化学势趋于相等,就像水最终静止在一个水平面上。
化学势(μ)在数学上定义为:
其中G是吉布斯自由能,n是摩尔数,T是温度,P是压力。即在恒温恒压下,系统每增加一摩尔某组分,G的增加量就是该组分的化学势。
化学势在生物系统中的作用
在我们的身体中,化学势差推动着许多重要的生理过程。血液循环系统就是一个典型的例子:当血液从心脏泵出后,氧气分子从动脉(血红蛋白含氧量高,化学势高)向组织细胞(化学势低)释放,实现氧气的有效输送。再如,在神经元传递信号时,钠钾离子的跨膜流动,也是由内外侧不同的化学势驱动形成的。而消化道的营养吸收,离子的渗透等过程,同样是化学势梯度引发的物质迁移,直接关系到生命活动的正常进行。
下表列举了几种常见的生命活动及其背后的化学势驱动力:
例如,人体肾脏通过调节钠、钾等离子的化学势平衡,精准地调控体内水分和渗透压,从而维持机体内环境的稳态。这一过程是通过肾单位中过滤、重吸收、分泌等机制实现的。肾脏能够感知血液中各种离子(如Na+、K+、Cl-等)的浓度变化,依靠化学势差主动转运离子,进而调节体液的渗透压与体积。
另外,在脱水或过量饮水时,肾脏都能根据内外部环境变化调整尿液的浓缩或稀释,保证细胞不会因渗透压失衡而受到损害,这充分体现了化学势原理在生命调控中的核心作用。
化学势与浓度的数学关系
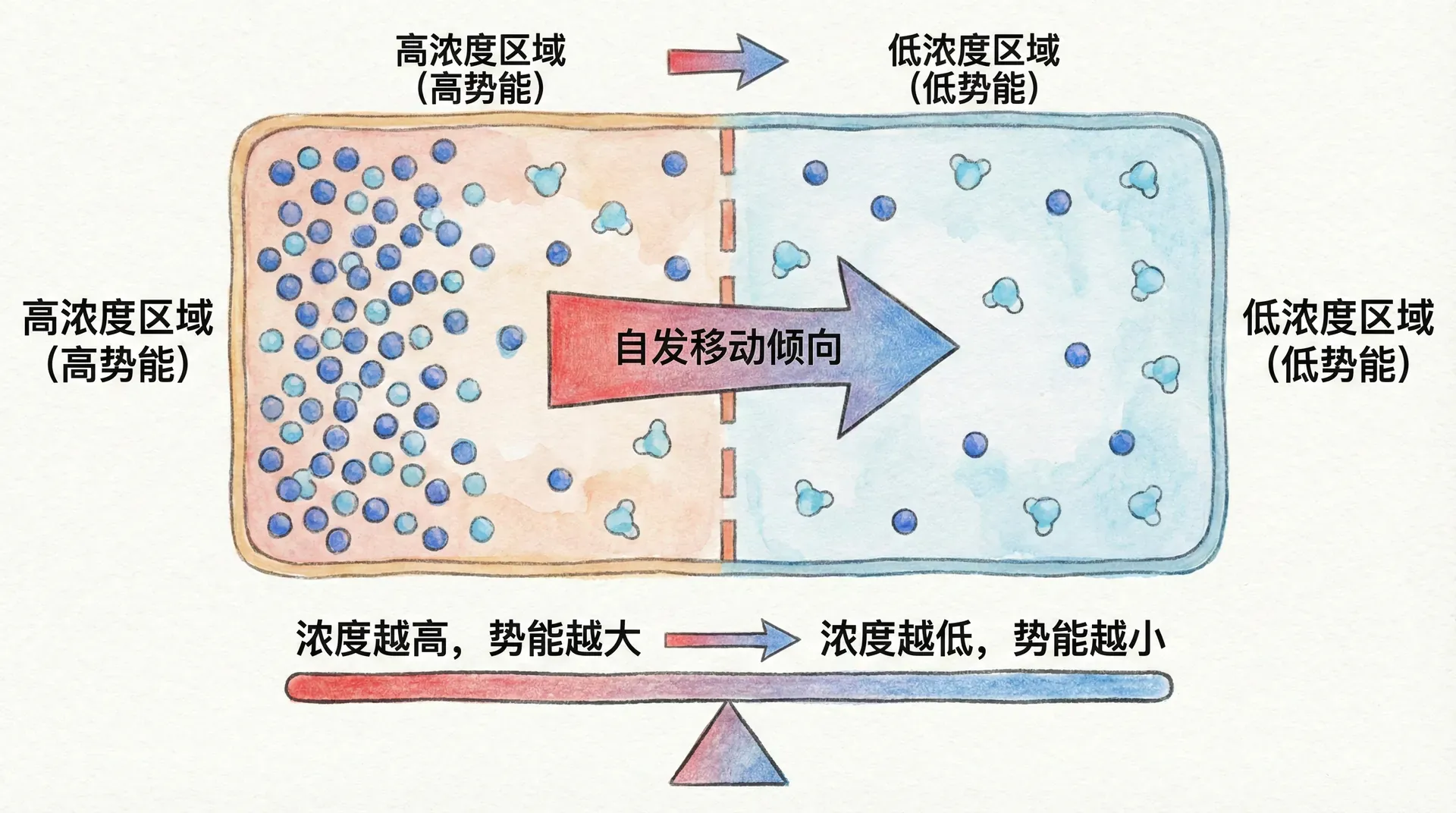
对数关系的推导与理解
化学势与物质浓度之间存在精确的数学关系。对于理想溶液,一种组分的化学势不仅由其类型决定,还与其浓度息息相关。其公式为:
其中μ°是标准化学势,R是气体常数,T是热力学温度,c是溶液中该组分的摩尔浓度。
这个对数关系揭示了一个物理规律:浓度的变化对化学势的影响是以对数形式体现的。举例来说,某种离子的浓度增加10倍,其化学势只会增加。在常温下(约298K),这个变化大约是5.7 kJ/mol,对分子行为具有重要影响。
这种数学关系不仅在实验室实际测算中非常重要,还决定了细胞和生物膜的许多过程,比如神经信号传导、主动转运、受体结合等,都根植于化学势的对数依赖性。
浓度梯度的实际应用
化学势与浓度之间的关系在医学和工程实践中有着广泛的应用。例如,中国传统医学中常用的“渗透压疗法”正是利用了这个原理:当用高浓度盐水敷在肿胀的伤口上,盐分子在伤口处形成高的化学势,促使细胞内的水分通过渗透作用流出细胞,从而减轻肿胀。类似地,现代医学中静脉注射生理盐水时,配制的盐水浓度与血液等渗,也是为了确保化学势平衡,防止细胞发生溶胀或脱水。
平衡常数与自由能
平衡常数的热力学基础
化学反应达到动态平衡时,反应物和产物的化学势变得相等,整个体系的自由能达到最小。此时,正逆反应速率相同,不再有“净变化”。在热力学上,反应的平衡常数K与标准自由能变化ΔG°之间具有如下关系:
这个公式不仅可以用来判断反应是否能够自发进行(ΔG°为负,即反应自发),还能根据实验测得的平衡常数反推出反应的能量特征。平衡常数K越大,ΔG°越负,说明反应朝生成物方向自发,反之亦然。
传统发酵工艺中的原理
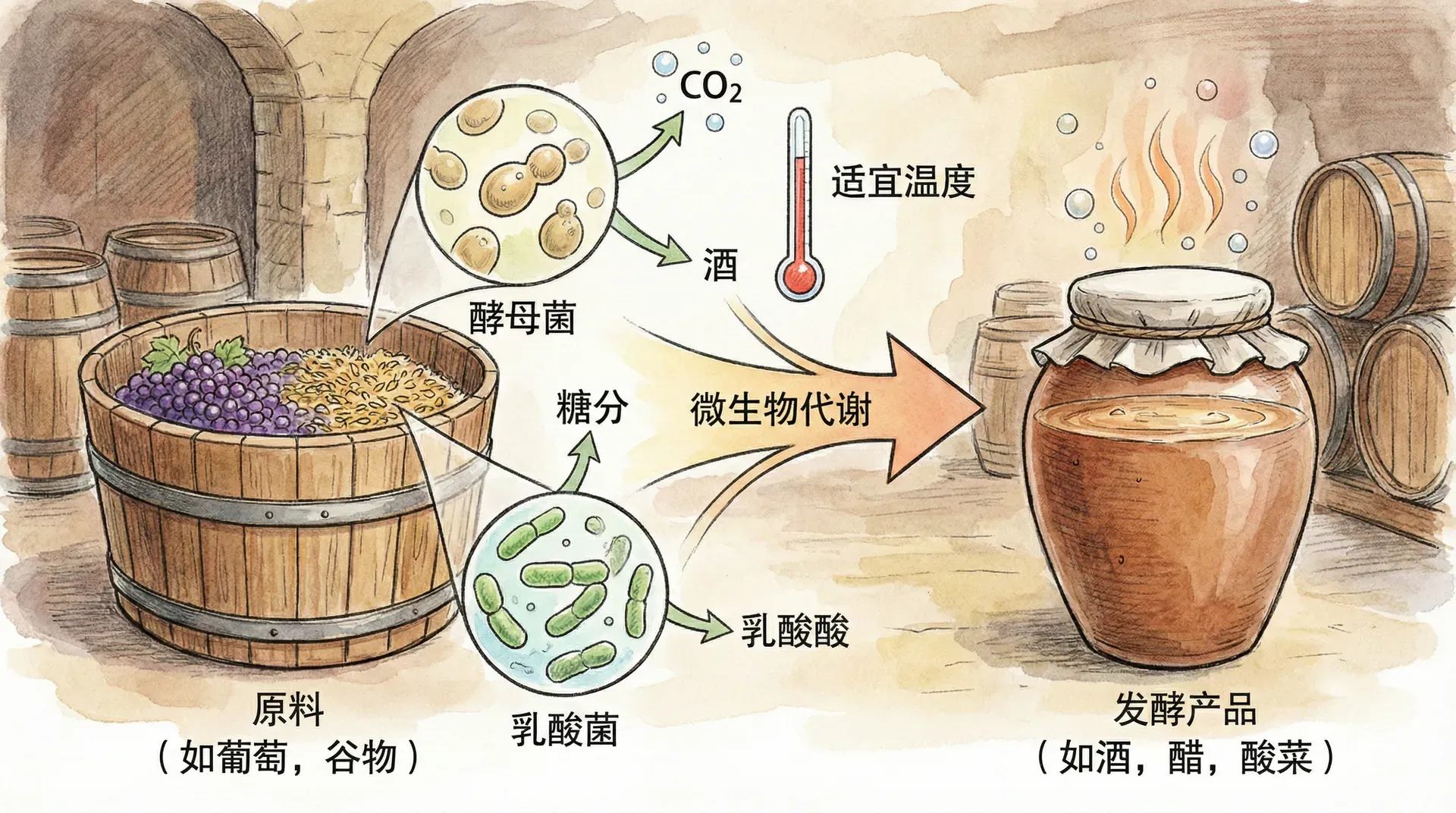
在传统的酱油、酒、醋等发酵工艺中,发酵过程的本质就是大量微生物催化下的化学反应逐步达到平衡。比如,在酱油的发酵中,蛋白质逐步分解为氨基酸、肽等小分子,这些反应的平衡常数受到温度、盐浓度、pH等因素影响。老酿造师傅通过调控这些条件,实际上利用了平衡常数与自由能的关系,从而影响终产物的滋味和品质。科学家研究发现,氨基酸等关键产物的浓度比值,正好等于对应反应的平衡常数,这为指导生产提供了理论基础。
亨德森-哈塞尔巴赫方程与缓冲系统
弱酸缓冲体系的数学描述
亨德森-哈塞尔巴赫方程是化学势概念在酸碱平衡中的一个重要而经典的应用。对于弱酸HA及其共轭碱A⁻组成的缓冲体系,方程如下:
这个方程本质上反映了质子在酸形式和碱形式之间的化学势平衡。当地溶液的pH等于酸的pKa时,意味着体系中酸和共轭碱的浓度相等,这也就是缓冲溶液缓冲能力最强的位置。这个定量关系为配制各类生物实验用缓冲液提供了理论指导。
亨德森-哈塞尔巴赫方程也常被用于推算药物在血液等生理液中的电荷状态,进而决定其活性和分布,为医学、药物化学等领域的实践操作提供支持。
人体血液的缓冲机制
人体血液中的碳酸-碳酸氢盐缓冲系统是维持血液pH稳定不可或缺的“防线”。该系统的pKa约为6.1,而正常血液pH为7.4。根据亨德森-哈塞尔巴赫方程:
推算可得,血液中碳酸氢根与碳酸的浓度比约为20:1。正是由于这种缓冲机制的存在,人体即使遇到轻微的酸性或碱性物质输入,血液的pH仍能维持在极窄的范围内(7.35-7.45),保证了细胞内各种酶和代谢的正常功能。如果缓冲系统功能失衡(比如慢性肾病或严重肺功能障碍),pH就会发生危险的波动,威胁生命安全。
不仅如此,体内还有磷酸缓冲系统、蛋白质缓冲系统等多重“保护伞”,共同稳固内环境,为生命活动保驾护航。
熵平衡
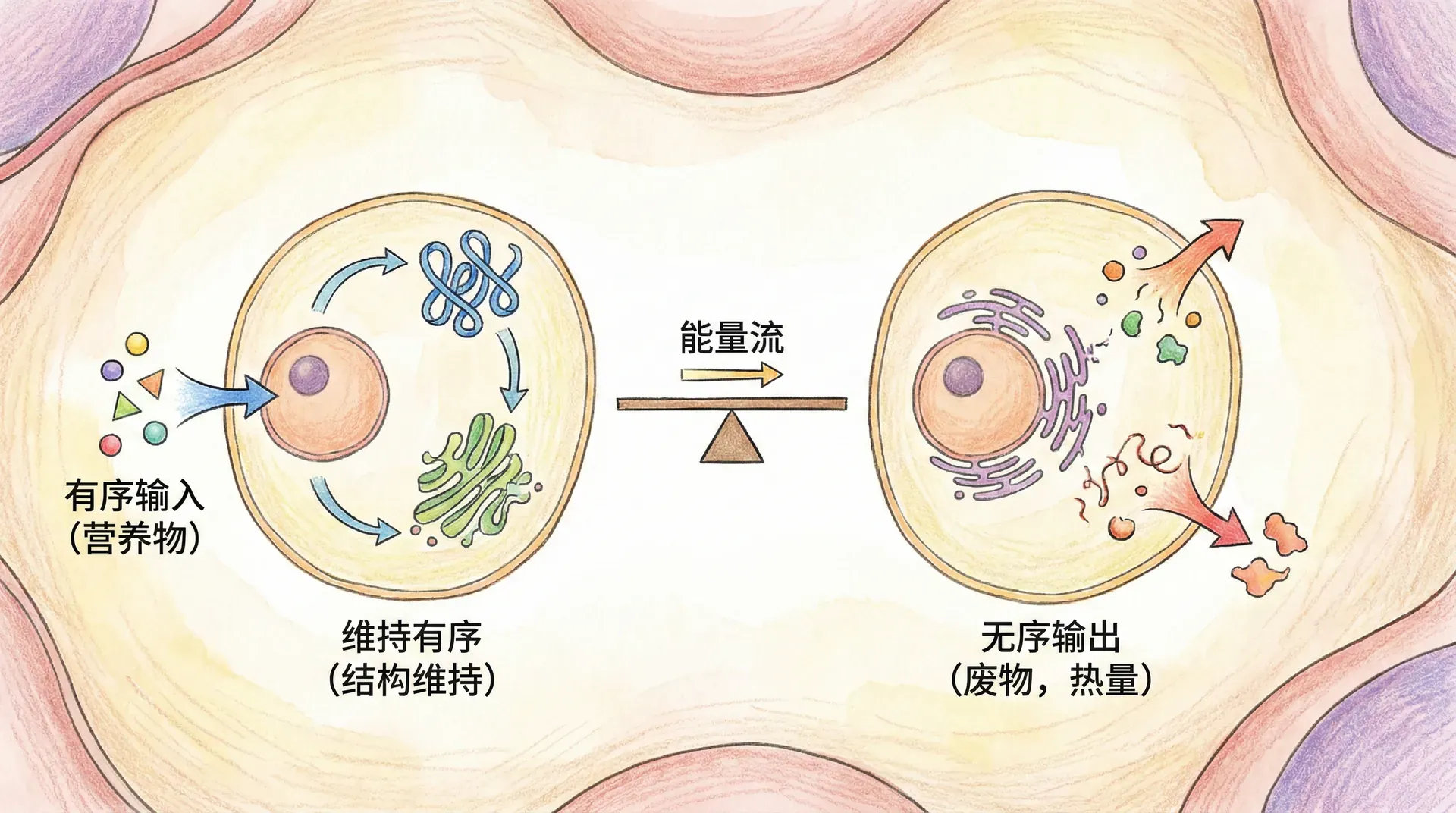
折叠驱动力的热力学分析
蛋白质折叠是一个高度复杂而精细调控的热力学过程,直接关系到生物体的功能与健康。折叠时,主链和侧链之间的各种相互作用——包括疏水作用、氢键、范德华力及静电相互作用——共同决定了蛋白质最终的三维结构。蛋白质折叠的自由能变化(ΔG)可以分解为焓变(ΔH)和熵变(ΔS)两个部分:
通常,蛋白质折叠的焓变部分并不总是有利(ΔH > 0),因为链内氢键和静电作用的形成,在一定程度上牺牲了蛋白质和水分之间更有利的相互作用。然而,折叠过程中,大量有序排列的水分子由于疏水残基聚集被释放回溶液,从而导致系统的熵大幅上升(ΔS > 0),这个熵效应往往成为蛋白质折叠的主要驱动力。
蛋白质天然状态的稳定性,是多项热力学贡献(焓与熵)较小数值的差值。其中,疏水效应导致全局系统熵大增,补偿了局部蛋白质结构构建带来的熵损失。只有当ΔG小于零时,蛋白质自发折叠。热力学对蛋白折叠的研究,还为蛋白质设计、疾病机理与治疗(如淀粉样变性相关的疾病)提供理论依据。
疏水效应的熵驱动机制
在蛋白质折叠机制中,疏水效应被认为是最重要的驱动力之一。疏水性氨基酸侧链往往趋于聚集到蛋白质分子的内部区域,避免与水直接接触。这一现象的本质并不在于疏水基团彼此之间有特殊“吸引力”,而是在于水分子的排列——当疏水残基暴露于水环境时,周围的水分子倾向于形成有序“包裹”,即所谓的“冰山结构”,以最小化接触面积。这导致水分子的熵下降。蛋白质折叠时,疏水残基聚集,把水分子“推出去”,这些水分子恢复了较高的无序状态,极大提升了系统的熵,成为巨大的自由能驱动力。
例如,中国饮食文化中的豆腐:大豆蛋白在卤水等盐分作用下发生收缩凝聚,实际上就是疏水效应的大规模体现。蛋白分子聚集成网状,水分子被排除,最终形成我们所熟悉的有韧性结构。类似的原理也应用于牛奶制成奶酪、鱼糜制成鱼豆腐等传统食品的加工。
各类相互作用在蛋白质折叠中的热力学贡献
蛋白质折叠的实时动力学和过程还受到分子伴侣、热休克蛋白等调控因子的影响。理解这些热力学规律,有助于精准干预相关疾病或开发药物。
量热法
差示扫描量热法的原理
差示扫描量热法(DSC)是现代生物物理学和生物化学中研究蛋白质折叠与稳定性的重要实验手段。通过同步加热待测样本和参比液体,并精确比较两者之间的热流差,就可以获得蛋白质在不同温度下的热容变化。当蛋白折叠或去折叠发生时,样本吸收或释放热量,会在DSC曲线上出现特征峰。
一个典型的DSC实验过程中,随着温度逐步升高,蛋白质会在特定温度(称为熔融温度Tm)发生去折叠转变。此时主链断开、二级结构解体,热量的吸收导致热容Cp急剧上升。通过DSC实验记录的精准热容曲线,可分别获得蛋白质折叠时的焓变(ΔH)、熵变(ΔS)和自由能变化(ΔG)等热力学参数,为蛋白折叠机制与稳定性评估提供了定量依据。
中国科学院在蛋白质研究中的贡献
中国科学院等国内顶尖科研单位,在蛋白质折叠与稳定性的实验研究中取得了许多原创成果。例如,中科院生物物理研究所发展出高通量DSC平台,系统筛查了多类植物蛋白、海洋蛋白及工程蛋白,发现了中国本土特色蛋白的独特熔融行为与环境适应机制。相关研究已在合成生物学和抗逆蛋白材料开发领域产生积极影响。
此外,国内科研团队基于DSC实验结果,提出了多温区熵-焓耦合机制、耐高温与高盐蛋白的分子设计方法,为我国在高性能生物材料、环保酶制剂等产业自主创新提供了重要理论支撑。
实验数据的热力学解析
DSC曲线不仅可以直观展示蛋白质在加热过程中的构象转变,还为分析其热稳定性提供了数据基础。在熔融温度Tm处,折叠态和去折叠态的自由能相等(ΔG = 0),其热平衡关系为:
其中ΔH_m表示在Tm处测得的焓变,ΔS_m为对应的熵变。DSC曲线下的面积即为吸收(或释放)的总热量,通过积分方法可进一步推算不同温度下蛋白质折叠与解折叠的自由能变化,揭示蛋白结构的稳定性、可逆性及折叠障碍。
实际应用中,DSC还能用于检测蛋白药物制剂的稳定性、筛查突变体蛋白的热力学性质,乃至用于生物材料的热响应评估。通过DSC,研究者能更全面地把握蛋白质与环境变化的关系与生命分子的物质基础。
化学势在生物技术中的应用
在现代药物设计和生物制造等领域,化学势已经成为指导分子优化与工艺提升的重要工具。一方面,药物分子与靶蛋白的结合本质上是一种化学势平衡与能量最小化的过程。通过定量计算不同修饰对分子化学势的影响,研发人员能够精准设计药物结构,提高其结合亲和力与选择性,减少副作用。例如,近年来许多创新药物的开发都采用了计算化学势的方法,显著降低了实验筛选成本,同时对于中药活性成分在体内分布和代谢机制的研究,也越来越多地借助化学势梯度进行解析,为药理机制阐明和精准医学提供理论依据。
另一方面,在生物制造和发酵工业领域,化学势理论的应用极大提升了生产过程的效率和可控性。工程师可以根据反应混合物各组分的化学势,优化底物转化率、提高产率并减少副产物。在中国生物燃料、生物塑料、医药发酵等新兴产业,越来越多企业通过化学势一体化模拟以及与自动化系统的结合,实现了连续发酵、动态调控等先进技术,不仅提升了资源利用率,还增强了过程的稳定性与环境友好性。
化学势作为连接微观分子机制和宏观生物过程的关键纽带,正推动医药、材料、生物工业等多个领域的创新发展。深入理解和灵活应用这一理论,将为生命科学与技术进步打开更广阔的空间。