基因的变化
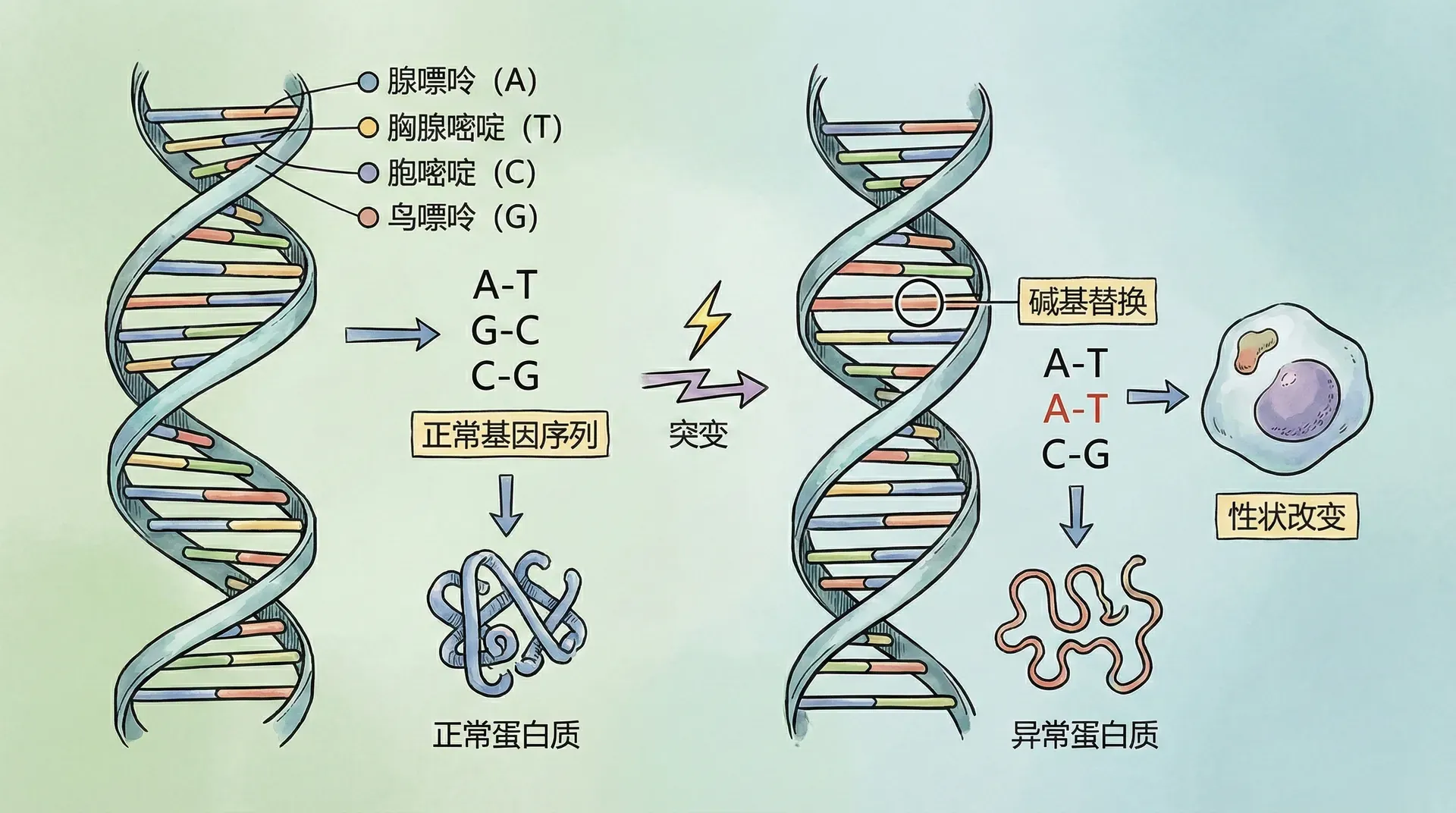
在我们的身体里,每一个细胞都像是一座精密的小工厂,日复一日地完成着无数复杂的任务。每个细胞的正常运行,都离不开深藏在其中的核心“控制系统”——基因。基因像一本详尽的说明书,把我们从父母那里继承来的所有生命密码,一字不差地记录在细胞的染色体中。这些密码决定了我们的外貌、健康,甚至某些性格特征。然而,这套遗传说明书其实远没有想象中那么“固若金汤”。在细胞分裂、DNA复制的漫长过程中,哪怕复制机制再怎么精密,也难以做到百分之百的无误。每当细胞进行分裂,它都要先把自己的全部基因“抄写”一遍,而在这个过程中,偶尔会出现一些“错别字”,这些微小的抄写错误我们就称为基因突变。
你也许会担心,这种突变是不是总会带来坏处?其实,事情远比想象中复杂。突变不仅仅是疾病和缺陷的来源,它其实也是生命多样性和进化的根本动力。大部分突变对生物体没有什么明显影响,甚至被悄无声息地带入下一代。而正是这些在基因上的一点点小变化,才让不同的个体产生差异,也让整个物种在漫长的历史进程中不断适应环境、演化提升。假如没有基因突变,无论是变色的花朵、还是会飞的蝙蝠,甚至我们人类自己,都不会像现在这样丰富和独特。
因此,从更宏观的角度来看,基因的变化像是自然的“创造力”。它让一成不变的生命蓝图拥有了无限的可能性,在地球这个巨大的舞台上,演绎出千姿百态的生物世界。
突变的发现与本质
19世纪末到20世纪初,科学家们在研究果蝇遗传时,发现了这样一件新奇的事情:即使在完全相同的环境下,一些果蝇的眼睛突然变成了白色,翅膀变短了,体型也有所不同。这些“特殊果蝇”引起了大家的兴趣。可即使用最精密的显微镜去观察它们的染色体,还是找不到明显的结构差异。这一发现表明:基因的改变,往往发生在染色体内部极其微小的位置,远远超出了肉眼和普通显微镜的分辨能力。
那么,这种微小变化究竟发生在什么层面?事实上,基因突变的本质就是基因在复制时偶尔出现的“抄写错误”。每当细胞分裂,遗传信息就要被完整地复制一遍。虽然细胞的复制机制已经非常精准,但依然无法确保丝毫不差。偶然情况下,一两个碱基对发生了变化,这就是突变的起点。这种发生突变后的基因,通常被称为新的“等位基因”,与原始基因在功能上可能有所不同。
以下总结了基因突变的一些基本特点:
有趣的是,突变后的基因往往并不“罢工”,它们依然可以自我复制,把新的遗传信息带到后代身上。如果突变位于生殖细胞(如精子、卵细胞)中,后代就有机会继承这种变化。当这种变化是显性的,下一代就能很快在外观或特征上表现出来;而如果它是隐性的,则可能隐藏不显,只有在偶然遇到同类突变后代纯合时才会表现。
你可能会好奇:突变到底有多稀少?其实,这种“意外”比想象中频繁。科学估算表明,人类每个基因每次复制发生突变的概率,大约为十万分之一。看起来很低,但考虑到人体有2万多个基因,身体每天有无数细胞分裂、复制,再加上地球上的人口基数,全球每天都在发生着数以亿计的新的基因突变。比如,某些家族性遗传病(如某型耳聋)每年在中国就能监测到数千个新发突变病例。
基因突变是生命常态。平均每个基因十万次复制会发生一次突变,足以让群体世世代代有新的遗传变异出现。
突变与进化的纽带
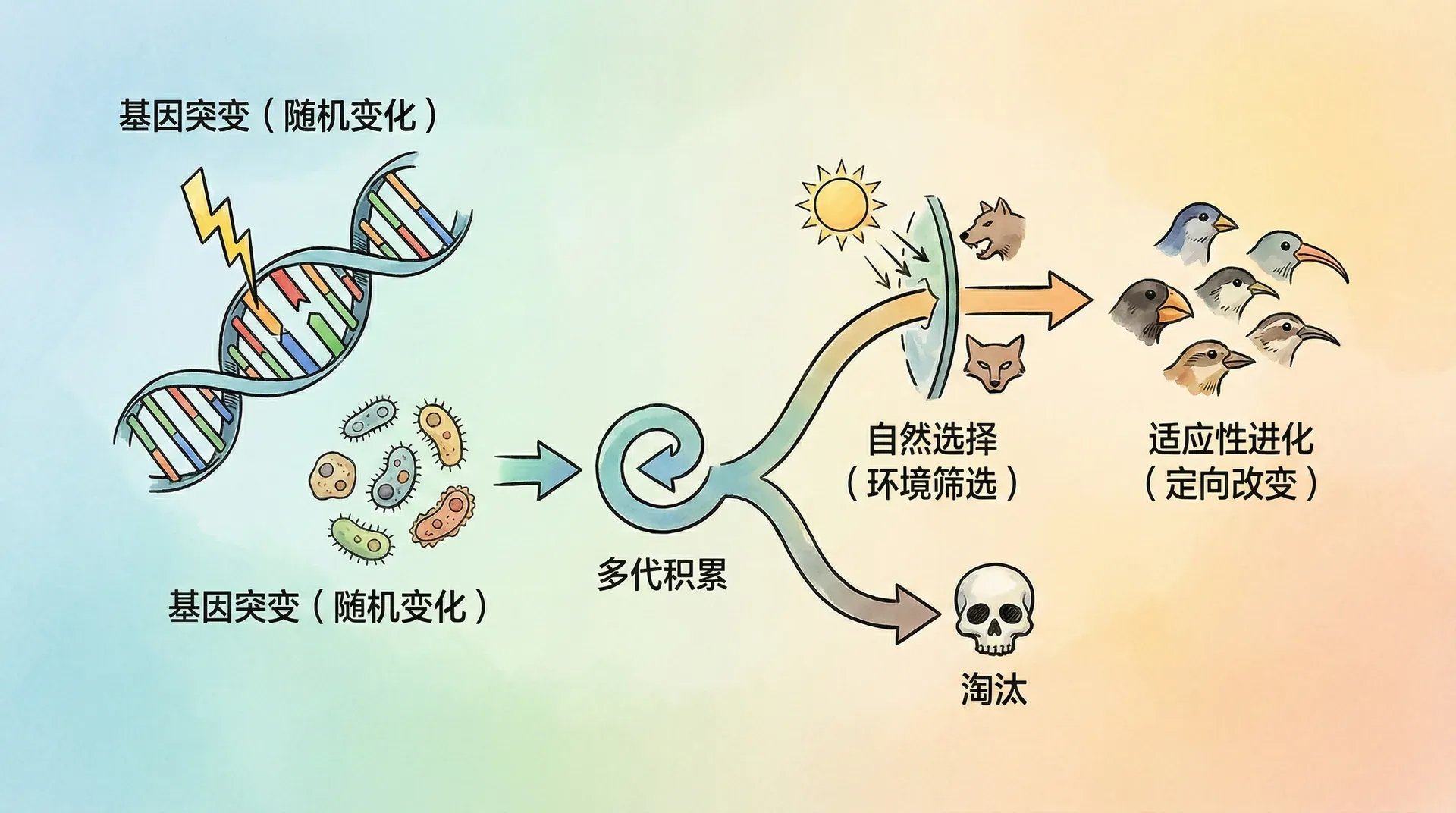
基因突变是进化的原材料。突变的作用,不仅仅是让个体之间变得“不一样”,更是生物演化的重要推动力。不同的突变会带来不同的影响,大致可以分为三类:
- 有害突变:降低生存/繁殖能力。例如:导致遗传性疾病的基因变异。
- 中性突变:对生存影响不大,表现差别微弱。例如:人体多处“沉默突变”,如一些血型小差异。
- 有益突变:提升适应能力,使个体更适合环境。例如:某些农作物自然产生抗病虫的基因。
下面图表归纳了三类突变及各自的例子:
虽然有益突变很少,但正是这极少数的幸运变异,在自然选择的推动下被保留,最终改变了物种的特征。那些有害突变,大多数会被逐渐淘汰。以人类为例,镰刀型细胞贫血就是一个经典“杂合优势”例子:虽然镰刀型基因纯合会导致疾病,但杂合基因却让携带者对疟疾有较强抗性,因此在疟疾流行区的频率比其他地区高很多。
20世纪,科学家们在实验室条件下首次系统探究了突变的机制。1927年,美国科学家赫尔曼·穆勒用X射线照射果蝇,发现突变率迅速升高,但突变类型与自然情形非常类似。这一发现证明:外界物理或化学因素能显著增加突变数量,但不会“制造”全新类型的变异。后来,人们又用紫外线、化学药剂(如EMS)等探索突变规律,并将这些成果应用于动植物育种和遗传病研究。
此外,突变率和累积速度也可以用数据和图表更直观地体现出来:
小结:
- 突变是生命多样性的基础。 如果没有基因突变,地球上的生物只能一成不变。
- 突变类型多样,效果千差万别。 大多数无害或有害,只有极少数能造福群体。
- 通过对突变的主动干预,人类加速了品种改良和疾病研究。
随着遗传学技术进步,我们将能更加精确地理解和利用突变,为医学、农业和人类未来带来更多可能。
人类遗传病中的突变印记
当我们谈论基因突变时,最直接影响我们的,莫过于那些发生在人类自身、并导致遗传性疾病的突变。这些遗传病给患者和家庭带来巨大挑战,同时也为我们研究基因如何在人类中遗传与变异提供了宝贵的“活标本”。许多著名的疾病正是自然界突变、自然选择和群体遗传的缩影。
蚕豆病(G6PD缺乏症)
蚕豆病广泛存在于中国南方,尤其是在长江以南和云贵等地。它的全称是葡萄糖-6-磷酸脱氢酶(G6PD)缺乏症。这类患者因缺少关键的G6PD酶,遇到蚕豆或某些药物时,红细胞无法抵御氧化损伤,会出现急性溶血危机,表现为尿色加深、严重贫血、乏力,甚至危及生命。
蚕豆病为典型的X染色体伴性隐性遗传。由于女性有两条X染色体(一条有缺陷,另一条多半正常,通常不发病),而男性只有一条X染色体(有缺陷就会发病),因此患者绝大多数为男性。即使家族无相关病史,也可能因为新的随机突变而产生患者。在南方部分地区,男性中G6PD缺乏症的患病率高达3-5%。
下面表格对比了常见的单基因遗传病的遗传方式:
举例说明:X连锁隐性遗传家系分析
假设母亲是携带者(XᴺXᵈ),父亲正常(XᴺY),则
- 儿子有50%概率患病(XᵈY);
- 女儿有50%概率为携带者(XᴺXᵈ),但极少发病。
地中海贫血(β-地贫)
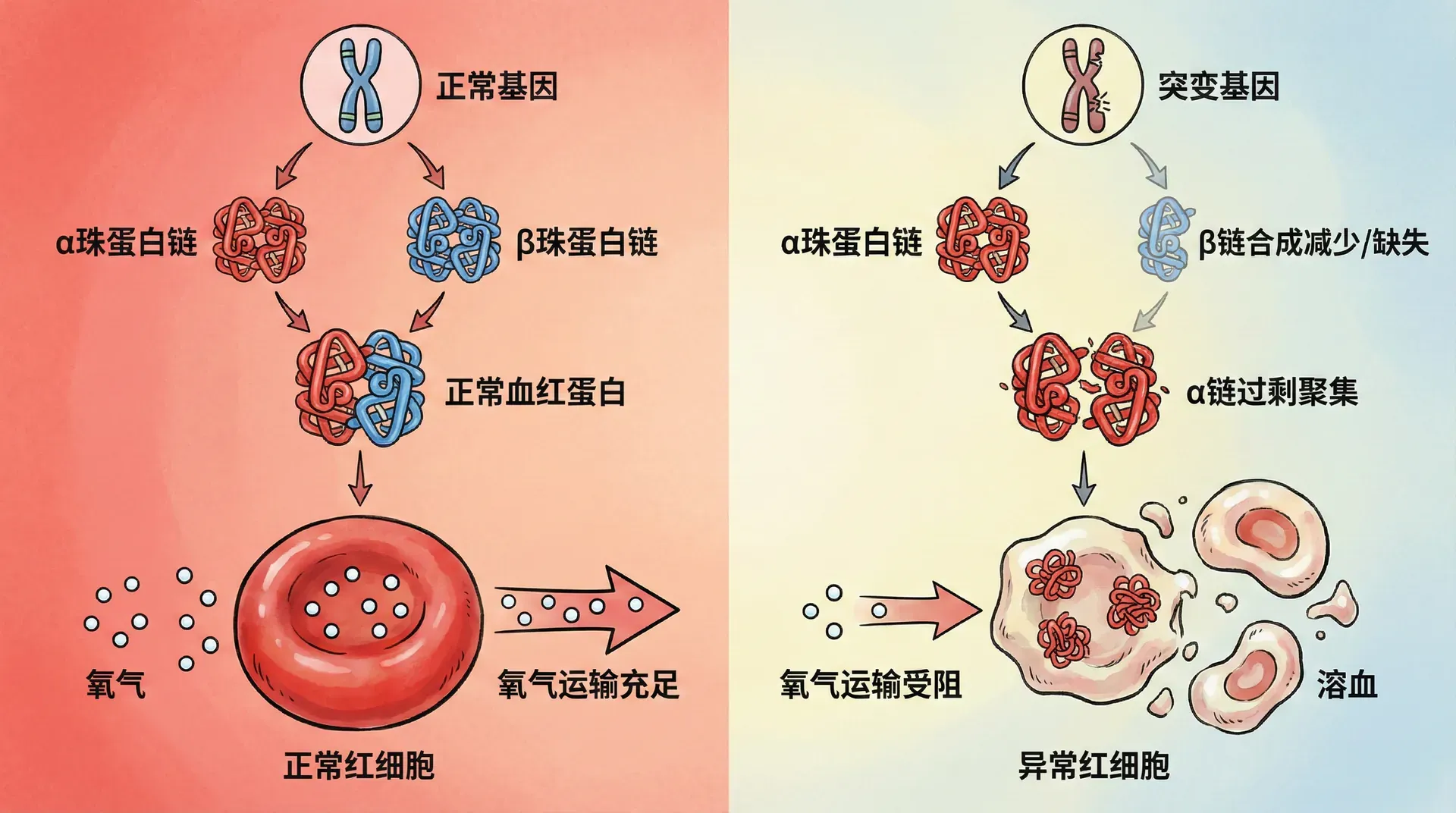
除了蚕豆病,地中海贫血同样在中国南方尤其是广东、广西、海南及云南等地高发。这种血液病是由于β-或α-珠蛋白基因突变所致,会导致血红蛋白生成障碍。纯合患者(从父母各遗传一份缺陷基因)通常在童年即表现出严重贫血,需频繁输血,生存受极大威胁。但杂合携带者(父母仅一方传递缺陷基因)多为正常人,仅有轻微贫血或无症状。
这种基因的高频率令人困惑。为什么即便重型患者难以成年生育,缺陷基因依然如此常见?科学研究表明——这可能与“杂合子优势”(heterozygote advantage)现象密切相关。
在疟疾流行地区,携带一份地中海贫血基因变异(杂合状态)的人,其红细胞对疟原虫的不适宜性给他们带来了防御优势。这有助于他们更好地抵御致死性疟疾,从而使相关突变遗传型在群体中长期保留。
地中海贫血与疟疾
这种遗传特性在全球范围内有不同表现:例如,非洲的镰刀型细胞贫血也是因为杂合子具有抗疟优势才在当地高发。
东南亚地区的“血红蛋白E”变体,则给主要食素人群带来利用铁的特殊优势。
囊性纤维化 & 遗传性耳聋
补充一个常见的常染色体隐性遗传例子——囊性纤维化(Cystic Fibrosis),在人口基数大的欧美国家中较为高发。该病需父母双方均为携带者,子女才有1/4概率患病(表现为呼吸、消化系统慢性病变)。
在中国,遗传性耳聋(如GJB2基因突变)属于常见常染色体隐性遗传病,典型特征为先天性双侧听力障碍。
随着现代遗传检测技术的普及,中国已有多省市在婚检、孕检中纳入了遗传病筛查,比如地中海贫血、G6PD缺乏症及耳聋易感基因等,这极大降低了新生重型遗传病发病率,为家庭和社会减轻了负担。未来,更多疾病的致病基因及其作用机制会被发现和阐明。遗传病给人类带来的痛苦,也激励我们不懈探索“看不见的遗传密码”。
体细胞突变与癌症
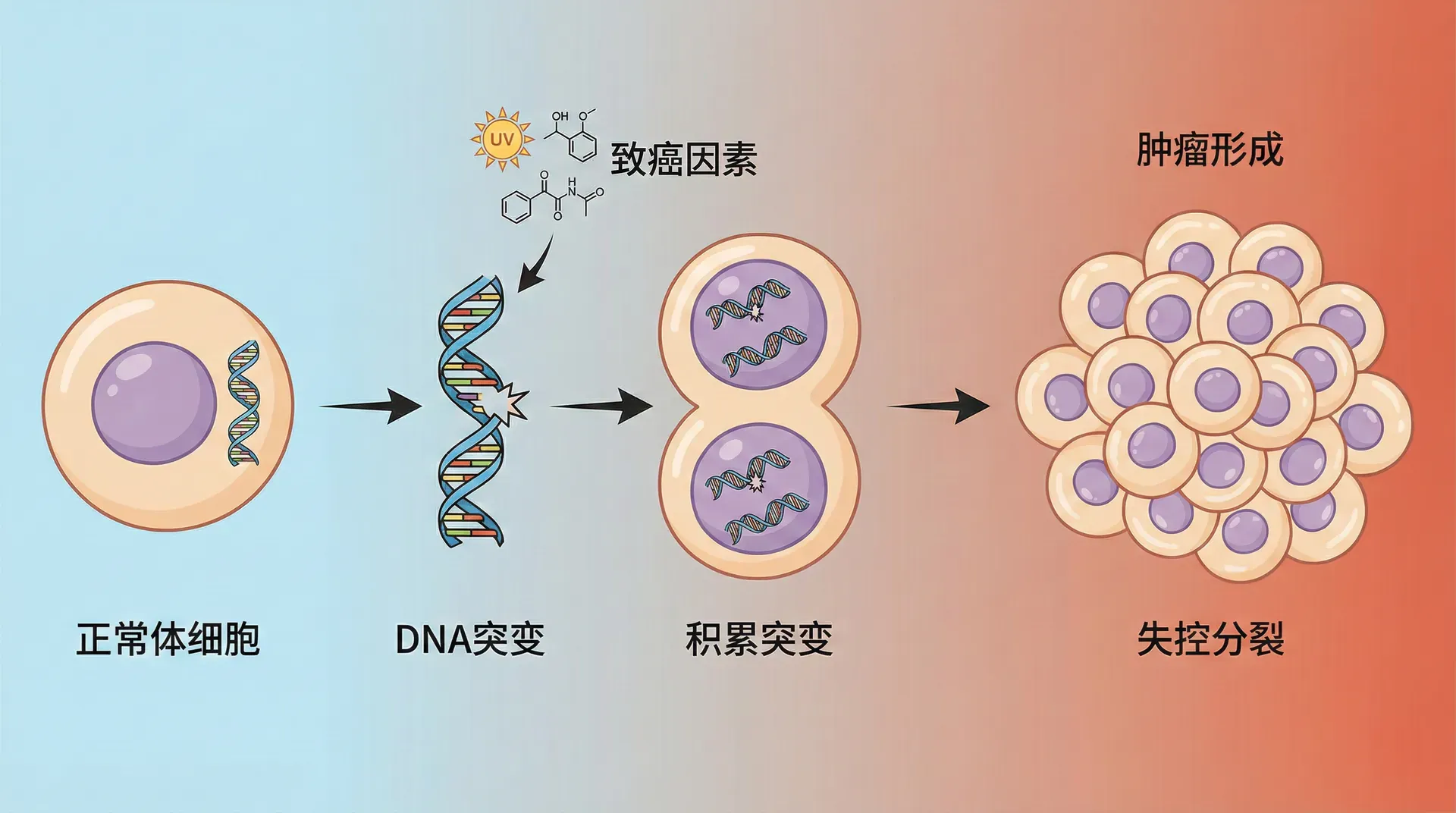
前面讨论的突变主要涉及生殖细胞,也就是精子和卵子。这些突变能够遗传给下一代,影响整个家族的基因库。但是,突变不仅仅发生在生殖细胞,还有另一大类称为体细胞突变,它发生在身体的普通细胞中。
我们的身体由约37万亿个细胞构成,这些细胞每天都在经历分裂和更新。例如,皮肤细胞不断脱落和再生,肠道内壁的细胞每隔几天就会全部替换,新血细胞也在骨髓中持续产生。每一次细胞分裂时,DNA都要复制一次,而这个过程有可能因偶发的错误而发生突变。由于这些体细胞突变不会影响卵子或精子,因此不能遗传给下一代,但它们会在个体体内积累,对健康产生重大影响。
以下对比了生殖细胞突变和体细胞突变的主要区别:
体细胞突变在正常情况下经常发生,但多数不会造成危害。不过,如果突变恰好出现在与细胞生长、分裂有关的关键基因上(比如抑癌基因或原癌基因),就可能让细胞失去生长控制,出现“失控分裂”,最终形成肿瘤。癌症的发生本质上就是体细胞突变的结果——一个突变的基因导致某个细胞无限制地增殖,并把缺陷遗传给其后代细胞,逐步形成可见的肿瘤。
导致体细胞突变的外部因素有很多,最主要的包括:
例如,自1895年X射线被发现不久,就有科学家因长期暴露染上了癌症,用生命的代价揭示出辐射的危害。著名的科学家玛丽·居里及其女儿长期从事放射性物质研究,最后均死于白血病(一种血液系统癌症)。而现代社会中,煤炭、石油、香烟的不完全燃烧释放的多环芳烃等化学物质也是公认的致癌物,吸烟者患肺癌的风险远高于不吸烟者。
值得说明的是,不是所有体细胞突变都会导致癌症。一个细胞要从正常转变为癌细胞,往往需要多个关键基因先后突变,再加上免疫系统失误,才会形成恶性肿瘤。人体自身也有各种DNA修复机制和免疫监控,大部分异常细胞会被及时清除。只有当防御机制失效、累积的基因损伤达到一定程度,癌症才有可能出现。
保护基因稳定性、减少不必要的突变诱因是维护健康的重要一环。这包括避免长期暴露在射线、致癌化学物质等高风险环境,养成良好的生活习惯,定期体检等。从这个角度来看,基因突变与我们的日常生活密切相关,科学认知和自我防护缺一不可。
从细胞到分子
通过细胞学与遗传学的发展,我们已经揭示了遗传信息储存在染色体上的基因中,也理解了基因突变如何带来变异并在自然选择中实现优胜劣汰。利用显微镜和遗传学实验,科学家不仅看到了细胞结构和染色体行为,还追踪了性状如何一代代传递,初步解读了生命延续的奥秘。
但每一步探索的深入又带来了新的疑问:基因究竟以何种形式存在于细胞之中?它们如何指导蛋白质合成并影响生物性状?微小的基因变化又为何会导致明显的个体差异?在一次次细胞分裂和DNA复制中,基因是如何高精度传递的,同时为何偶尔也会出错?显然,传统细胞学和遗传学已无法满足人类对生命本质的好奇心。
于是,科学家们的目光转向更微观的分子层面。这里,旧有的观察工具已难以奏效,需要依赖生物化学与物理学的新方法。从细胞结构到分子层面的探索,人们逐渐认识到,生命的奥秘深藏于细胞内携带遗传信息的化学物质之中——它们的本质、结构和遗传机制成为新的研究核心。
破解基因的本质与功能,需要跨越生物学、化学和物理学的边界,将多学科知识融会贯通。我们正在经历一场由大自然观察者到分子探秘者的重大转折,也以全新分子的视角重新解释生命现象,继续追问“生命是什么”这一终极问题。