质量测量原理
在生物技术实验室中,准确的测量是获得可靠实验结果的基础。无论是称量试剂、测定蛋白质浓度,还是分析DNA样品,每一个测量过程都会影响最终结果的质量和可信度。实验过程中,哪怕是看似微小的失误或仪器偏差,都有可能导致数据出现较大偏差,进而影响实验结论。
因此,理解质量测量的基本原理,不仅能帮助我们正确选择和使用各类仪器设备,还能让我们科学地评估实验数据的有效性与重现性。掌握这些原理,有助于发现潜在的误差来源,提升实验设计的严谨性。本内容将从测量标准的建立、误差类型及分析方法,到不确定度的评估体系,系统地介绍实验室测量的核心概念,帮助读者构建扎实的质量控制基础。
测量标准与校准的重要性
在一家生物制药公司,质检人员小李每天需要用天平称量原料药。有一天,她发现同一批次的样品在不同天平上称量结果相差较大。经过检查发现,其中一台天平已经半年没有校准了。这个案例提醒我们,测量仪器的准确性需要通过定期校准来保证。
测量标准是指用于定义、实现、保存或复现某个物理量的量值的实物标准、测量仪器或测量系统。在我国,测量标准体系采用分级管理的方式。国家计量院负责维护国家基准,它代表了我国测量能力的最高水平。例如,中国计量科学研究院保存着质量的国家基准——一套不锈钢砝码组,其量值可以追溯到国际千克原器。
校准是指在规定条件下,为确定测量仪器所指示的量值与对应的已知量值之间关系的一组操作。校准的目的不是调整仪器,而是确定仪器的示值误差。
实验室仪器的校准通常分为外部校准和内部校准两种形式。外部校准由具有资质的第三方机构执行,校准证书具有法律效力。例如,上海某基因检测中心的分光光度计每年由当地计量所校准一次,校准报告详细记录了仪器在不同波长下的偏差值。内部校准则由实验室自行使用有证标准物质进行,频率更高,通常每周或每月进行。深圳一家细胞培养实验室使用标准砝码每周校准一次天平,确保称量结果的一致性。
校准与检定的区别常常被混淆。检定是由法定计量机构按照国家计量检定规程进行的强制性检查,合格后出具检定证书。而校准是非强制性的,主要目的是获得测量偏差数据。对于生物技术实验室的大多数仪器,校准比检定更为常用,因为校准更灵活,可以根据实验室的具体需求制定校准方案。
以下总结了校准与检定的主要差异:
溯源性
溯源性是指测量结果能够通过连续的比对链与适当的测量标准联系起来的特性。这个概念听起来抽象,但在实际工作中极为重要。如果广州、武汉、成都三个实验室同时测定一批疫苗的蛋白质含量,如何保证三地结果可以相互比较?答案就是溯源性。
测量溯源链从国际基准开始,经过国家基准、传递标准,最终到达实验室的工作仪器。以质量测量为例,国际千克原器保存在法国国际计量局,中国的国家千克基准通过国际比对与之建立联系,各省级计量院的质量标准再与国家基准比对,最后实验室的天平通过标准砝码与省级标准建立溯源关系。这样形成了一条完整的溯源链。
上面的图表清晰展示了测量溯源链的结构与准确度的逐级传递:从国际/国家标准开始,经过国家基准、校准实验室,最终到达日常使用的测量器具。每一级的传递都会引入新的不确定度,因此溯源链越长,准确度会逐步降低。但只要这种传递链条完整,最末端仪器的测量结果依然是可信的。这也是实验室要定期校准仪器的根本原因——通过校准确保本实验室的测量结果能够及时“重新连接”到上一级标准,保证测量的可靠性和溯源性。
在生物技术领域,溯源性的实现依赖于有证标准物质。例如,杭州某生物公司测定蛋白质浓度时使用牛血清白蛋白标准品,该标准品的浓度值由国家标准物质中心认证,其量值最终可追溯到纯物质的质量基准。没有这种有证标准物质,实验室之间的测量结果将无法比较。
建立溯源性需要实验室做好文件记录工作。仪器的校准证书、标准物质的证书、校准操作的记录,这些文档共同构成了溯源性的证据链。苏州一家第三方检测机构在接受ISO 17025认可审核时,审核员重点检查了溯源性文件,包括移液器校准记录、标准品购买凭证、以及溯源路径图。完整的文档记录不仅是质量管理的要求,更是测量结果可靠性的保障。
测量误差的来源与分类
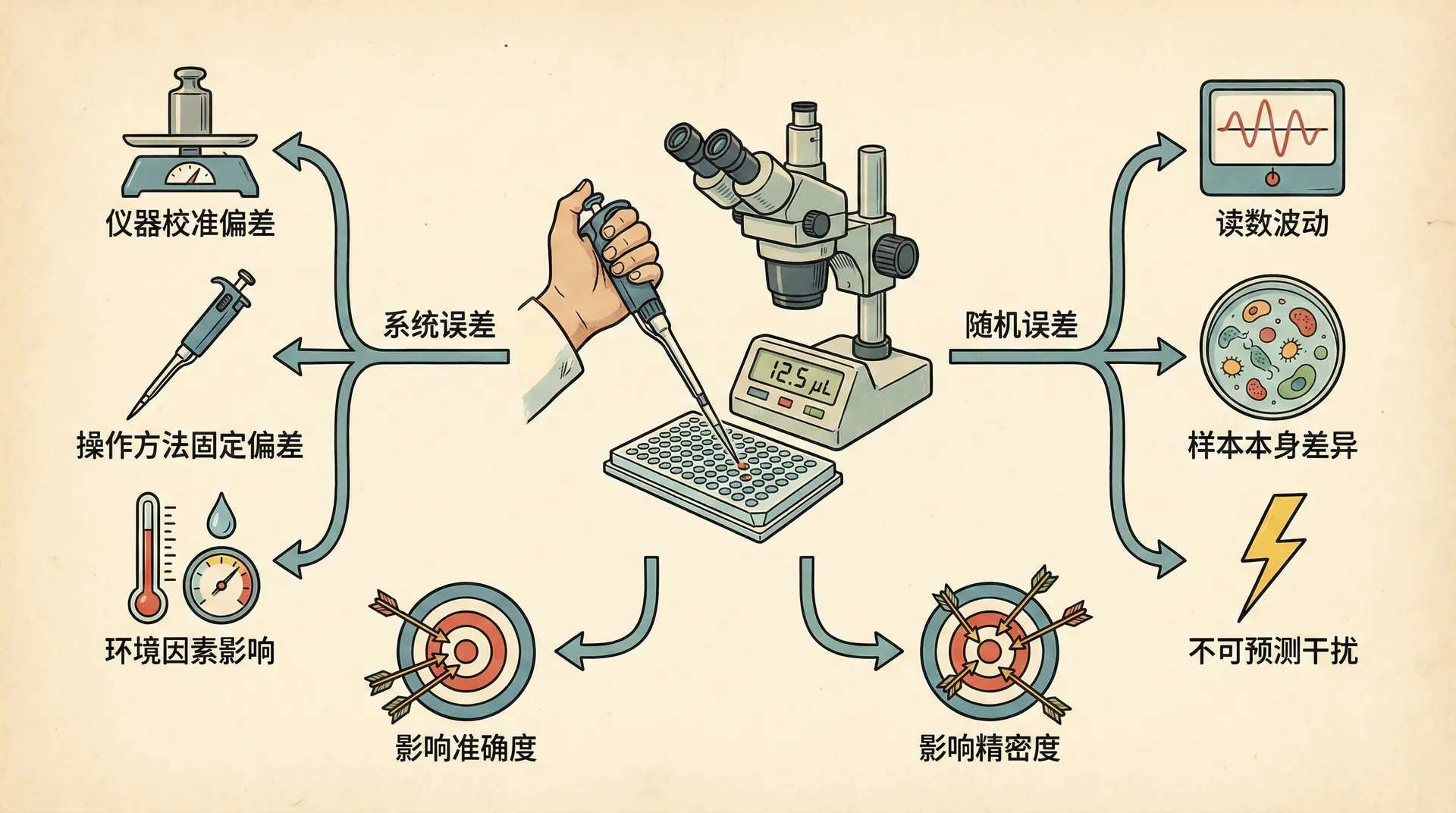
在微生物实验室里,学生小张用移液器移取了十次1.0 mL的溶液,用天平称重后发现结果从0.996 g到1.004 g不等。为什么会出现这种差异?这就涉及测量误差的问题。
测量误差是指测量结果与被测量真值之间的差异。理解误差的性质有助于我们采取适当的措施减小误差影响。测量误差按其性质可分为系统误差、随机误差和粗大误差三类。
系统误差在相同测量条件下重复测量时,其大小和符号保持不变,或按可预知规律变化。比如天平零点漂移导致所有称量结果偏高0.002 g,这就是典型的系统误差。在西安一家制药厂,技术人员发现pH计总是比标准溶液的pH值低0.1个单位,经检查是电极老化所致。系统误差的特点是具有重复性,因此可以通过校准、修正等方法减小或消除。
随机误差是在相同条件下多次测量同一量时,因多种微小不可控因素(如环境温度波动、仪器灵敏度、操作者习惯等)随机变化,使得测量结果在一定范围内波动。此类误差虽然无法完全消除,但因其服从统计规律,可以通过增加测量次数、求平均值等方式来减小影响。
从上图可以看出,随机误差遵循正态分布规律:约68.27%的测量结果分布在平均值(μ)±1个标准差(σ)范围内,约95.45%分布在±2σ范围内,几乎所有数据(99.73%)都会落在±3σ之间。标准差越小说明误差越容易被控制,测量值更集中,重复性越好。因此,统计分析不仅能量化随机误差,也为判定测量结果的可靠性提供了依据。
粗大误差是指明显偏离实际值的误差,也称为异常值或离群值。这类误差通常由操作失误、仪器突发故障或环境条件剧变引起。例如,长沙某实验室在进行蛋白质定量时,一组数据中出现了一个比其他值高出三倍的结果,经查证是移液时吸入了气泡。粗大误差应通过严格的操作规程和数据审查来预防和剔除。
以下是三类误差的特征及处理方法:
误差的另一种分类方式是按表示方法分为绝对误差和相对误差。绝对误差是测量值与真值之差,具有量纲。相对误差是绝对误差与真值的比值,通常用百分数表示。郑州某实验室称量5.00 g样品,实际称得5.02 g,绝对误差为0.02 g,相对误差为0.4%。在评价不同量级的测量结果时,相对误差更有意义。
准确度与精密度
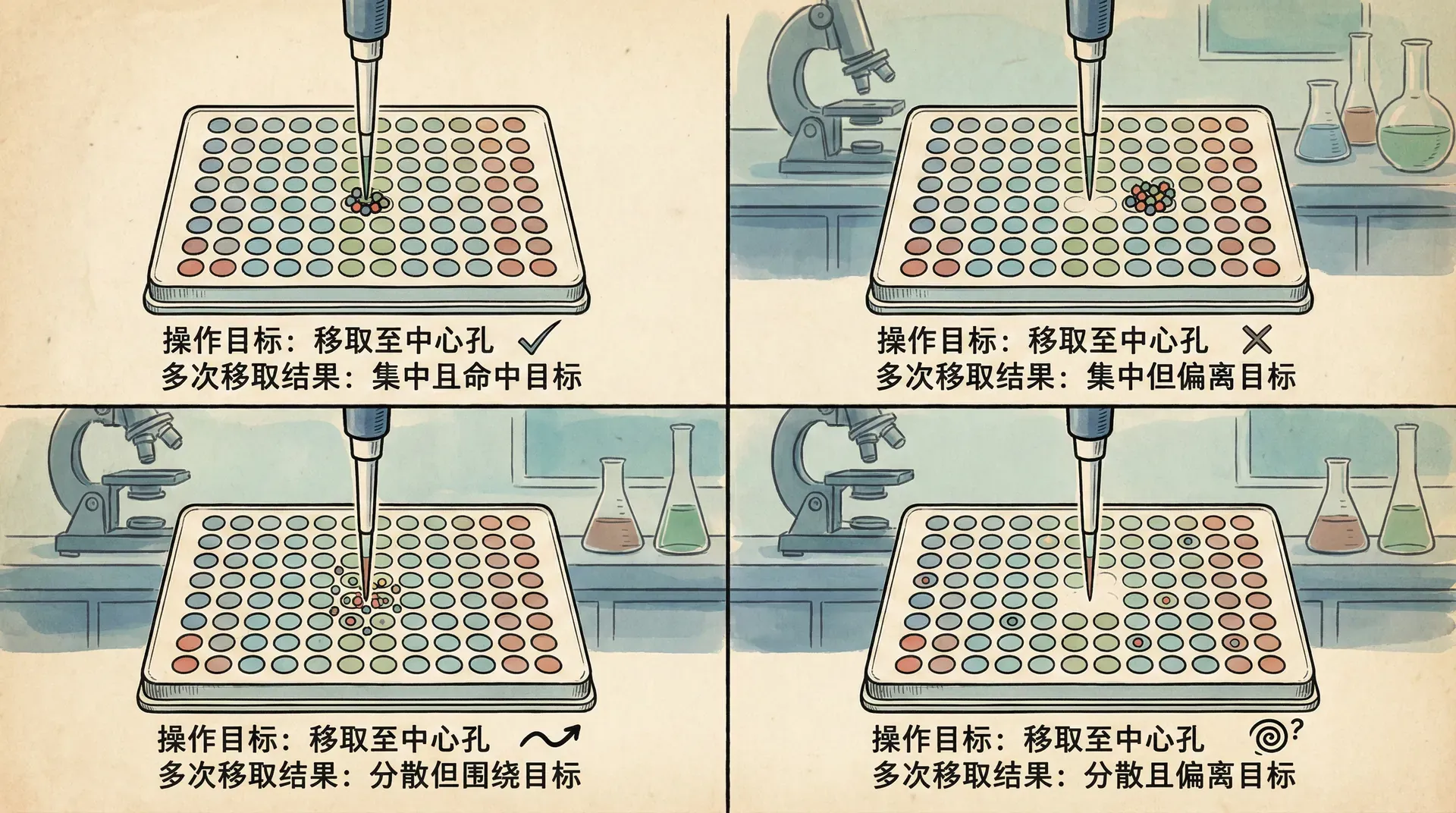
准确度和精密度是评价测量质量的两个基本概念,但它们常常被混淆。青岛某生物公司的质量经理用一个生动的比喻来培训员工:如果把测量比作射击,准确度是指弹着点接近靶心的程度,精密度是指弹着点彼此接近的程度。
准确度表示测量结果与真值的接近程度,反映了系统误差的大小。一个准确度高的测量方法,其测量值的平均值应接近真值。合肥某检测中心使用原子吸收光谱法测定水样中的铜含量,用有证标准物质验证,测定值与标准值的偏差小于2%,说明该方法准确度良好。准确度通常用相对误差或回收率来表示。例如,向样品中加入已知量的待测物质,测定加标后的总量,回收率=(测得增加量/加入量)×100%。理想的回收率应在95%-105%之间。
高精密度不代表高准确度。一个测量系统可能重复性很好,但如果存在未被发现的系统误差,所有测量值都可能偏离真值。
精密度是指在相同条件下重复多次测量时,各测量结果之间是否接近。如果每次测得的数值都非常接近(比如相差非常小),说明精密度高。但即使结果很接近,也不一定代表这些数值就是真实值。比如我们使用同一把尺子连续量取同一个物体的长度,五次读数都为10.2厘米、10.2厘米、10.1厘米、10.2厘米和10.1厘米,这说明你的测量精密度高(数据很接近),但如果这把尺子本身有误差,测量结果依旧可能不是实际长度。一些常用的精密度评估指标有标准差和变异系数等。
-
准确度 (Accuracy):测量平均值与真实值(靶心)接近的程度,反映系统误差大小。
-
精密度 (Precision):每次测得值间的接近程度,反映随机误差大小。
优化准确度主要需修正系统误差,如校准仪器、更换纯度更高的试剂等;提升精密度需减少随机误差,例如加强操作规范、稳定环境条件等。
上图用靶盘示意法直观展示了准确度和精密度的四种典型组合:圆心表示真值,圆点为多次测量值。第一象限(左上)代表理想测量——既准确又精密。第三象限(右下)则是最差情况——既不准确也不精密。注意第三种模式(低准确度高精密度)最易误导,因为数据结果很“集中”但实际都偏离了真值。
影响准确度的因素主要是系统误差,包括仪器零点偏移、试剂纯度不够、方法本身的固有误差等。天津某实验室发现分光光度计测定结果总是偏低,检查后发现比色皿有划痕影响了透光率。影响精密度的因素主要是随机误差,如环境温度波动、操作者技术熟练程度、样品均匀性等。沈阳某实验室在冬季供暖初期发现测定精密度下降,原来是室温波动过大影响了仪器稳定性。
提高准确度的关键措施包括定期校准仪器、使用高纯度试剂、采用标准方法、进行空白对照和加标回收实验等。提高精密度的方法包括严格控制实验条件、提高操作技术、增加平行样数量、选用高质量仪器等。在实际工作中,应根据测量目的合理确定所需的准确度和精密度水平。例如,用于判定合格与否的检测需要高准确度,而用于监测生产过程稳定性的测量则更注重精密度。
不确定度分析
在传统的误差理论中,我们假设存在一个“真值”,测量的目标是无限接近这个真值。但在实际工作中,真值往往是无法得知的。20世纪末,国际计量组织提出了测量不确定度的概念,为测量结果的质量评价提供了新的框架。
测量不确定度表征被测量值分散性的参数,反映了我们对测量结果可信程度的认识。与误差不同,不确定度不是测量值与真值的差,而是测量结果可能的变动范围。例如,武汉某实验室报告一个样品的蛋白质含量为25.6 mg/mL,不确定度为0.8 mg/mL(k=2),这意味着我们有约95%的把握认为真实含量在24.8到26.4 mg/mL之间。
完整的测量结果应包括测量值、测量单位和不确定度三个要素。只给出测量值而不给出不确定度,无法判断测量结果的质量。
测量不确定度的来源可分为两大类。A类不确定度通过对测量值的统计分析评定,主要来自随机效应。例如,厦门某实验室用移液器重复移取10次,计算标准差得到A类不确定度。B类不确定度通过非统计方法评定,基于经验、仪器说明书、校准证书等信息。比如,根据天平校准证书显示的最大允许误差,采用均匀分布假设计算B类不确定度。
不确定度评定的基本步骤包括建立测量模型、识别不确定度来源、量化各分量、合成标准不确定度、计算扩展不确定度。以生物实验室常见的溶液配制为例说明。昆明某实验室需要配制100 mL浓度为1.00 mg/mL的蛋白质标准溶液,步骤是称量100.0 mg标准品,溶解后定容至100 mL。
测量模型为:。
不确定度来源包括天平称量的不确定度、容量瓶定容的不确定度、标准品纯度的不确定度。假设天平校准证书显示不确定度为0.1 mg(k=2),则标准不确定度 u₁ = 0.1 ÷ 2 = 0.05 mg。容量瓶证书显示±0.10 mL(均匀分布),标准不确定度 u₂ = 0.10 ÷ (3 的平方根) ≈ 0.058 mL。标准品证书显示纯度99.5±0.3%(正态分布,k=2),标准不确定度 u₃ = 0.3 ÷ 2 = 0.15%。
上图展示了不同来源对总不确定度的贡献。可以看出纯度不确定度是主要因素,这提示我们选用高纯度标准品对提高测量质量最为关键。
合成标准不确定度采用不确定度传播定律计算。对于浓度 = 质量 / 体积这样的模型,相对合成不确定度为:
则标准不确定度 。
扩展不确定度 ,其中 为包含因子,通常取 ,对应约 的置信水平。因此 。最终结果表示为:蛋白质浓度 = 。
不确定度评定在实验室认可和质量管理中越来越重要。ISO 17025标准要求检测实验室具备评定测量不确定度的能力。兰州某第三方检测机构在申请CNAS认可时,针对每个检测项目编写了详细的不确定度评定程序,这不仅满足了认可要求,也提升了对测量过程的理解和控制能力。
下表对比了传统误差理论与不确定度理论的区别。
在生物技术实验室的日常工作中,完整评定每个测量的不确定度可能不现实,但至少应对关键测量项目进行不确定度评定。例如,用于产品放行检验的关键指标、用于仪器校准的参考值、以及要求很高准确度的研究性测量。南京某疫苗企业对疫苗效价测定建立了完整的不确定度评定程序,当测量值接近规格限时,通过比较不确定度范围与规格限,可以更科学地做出合格判定。
理解质量测量原理,不仅要掌握各种概念的定义,更重要的是能够在实际工作中应用这些原理来提高测量质量。无论是选择合适的仪器、制定科学的操作规程,还是正确评价测量结果,都离不开对测量原理的深刻理解。随着生物技术的发展,对测量质量的要求越来越高,掌握这些基本原理将为今后的学习和工作打下坚实基础。