病毒的奥秘
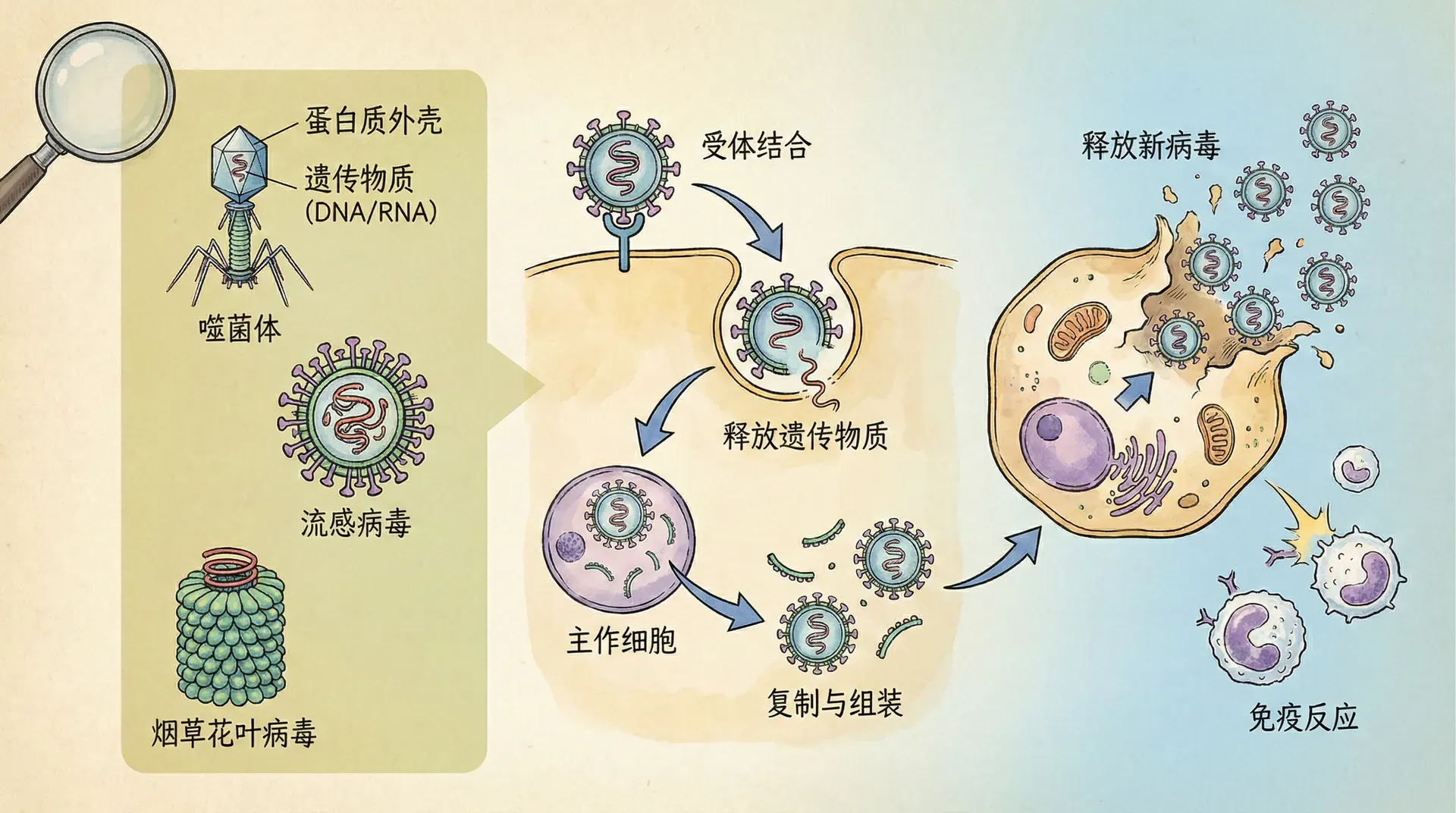
病毒是一类极其微小、结构简约但异常狡猾的生命体。它们广泛存在于自然界,无论是在海水、土壤,还是动物、植物甚至人类体内,都能发现它们的踪迹。虽然病毒无法独立生活,必须依赖寄主细胞来完成自身的复制,但正因这种独特的“寄生”方式,使得它们成为生物进化过程中的重要参与者和推动者。
从遗传物质来看,病毒拥有多样的基因类型——有的以DNA为载体,有的则以RNA为遗传基础,这决定了它们的繁殖方式与变异能力。例如,RNA病毒更容易发生突变,因此在流感、新冠等疾病的流行中常常出现新变种。这种高变异性既给防控带来了挑战,也加速了病毒与宿主的“军备竞赛”。
病毒的生命周期非常特殊:在离开宿主细胞时,基本处于无生命的“休眠”状态,当接触到合适的细胞后才会“激活”,释放遗传信息并劫持细胞的合成机器,批量制造出新的病毒颗粒。这种高效而隐蔽的模式,使得病毒时常成为全球疾病爆发的元凶。
认识病毒
在我们肉眼看不见的微观世界里,存在着一类特殊又神秘的“生物”——病毒。或许你难以想象,在你呼吸的空气、喝的水甚至常见的尘埃中,都可能藏着无数微小的病毒。它们无处不在,却又神出鬼没。与我们熟悉的细菌相比,病毒要更加简约,甚至严格来说,它们甚至算不上“完全的生命体”。病毒既不能像细菌那样独立生活,也不像动植物那样拥有完整的细胞结构。它们就像自然界的“寄生者”,必须依赖其他生物的细胞“借用”生命的机器来维持自身的存在和繁殖。
如果把细胞比作一个结构完善、功能齐全的现代化工厂,那么病毒则像是只带着图纸(遗传物质)和简单包装(衣壳蛋白)的“外包商”或“黑客”。它们没有自己的生产设备,也没有工人和能源系统,只能想方设法混入别人的工厂,利用现有的设备来制造自己的产品。正因为如此,病毒代表着生命的极致“简化”——抛弃所有多余,专注于遗传信息的存续和传播。
病毒是地球上最简单却也最扑朔迷离的生命形式。它们徘徊在生命与非生命的边界上,不断挑战和刷新我们对“生命”定义的理解。科学家对病毒的研究曾多次推动生物学理论的重大变革。
病毒的基本特征
病毒虽小,却拥有一套极具特色的生存密码。科学家借助高倍显微镜和分子手段,对病毒进行研究,发现它们具备一系列鲜明的特征。
首先,病毒的结构非常简单,主要由两个基本部分组成:遗传物质和蛋白质外壳。它们的遗传物质可能是DNA或者RNA——就像是存储有繁殖方法和“作战计划”的指令手册。蛋白质外壳则如同一层结实的“安全护甲”,不仅守护着遗传材料,也决定了病毒能感染哪些细胞类型。
与细胞生物相比,病毒没有细胞膜,缺乏细胞核和各种细胞器。没有线粒体,没有叶绿体——它们没有自己的能量工厂,对外部世界的响应能力极其有限。可以说,病毒像是生命的“最小单位”,只带着必要的遗传信息和最精炼的“包装”,专为高效入侵和复制而生。
从上图可以直观地看出,病毒的体型在所有活跃的微生物中最为微小,通常直径只有几十到几百纳米,远远小于细菌和典型的真核细胞。正因为如此,我们必须借助先进的电子显微镜才能观测和研究病毒的真实面貌。世界上最小的病毒甚至只有20纳米左右,仅为某些细菌的二百分之一。
病毒与细胞的本质区别
要深入理解病毒的独特性,我们可以将它与不同类型的细胞生物进行对比。虽然病毒和细胞生物都包含遗传物质,但两者在结构、功能和生活方式上有着本质区别。
可以看到,病毒最大的“弱点”就是离开宿主就几乎丧失一切活性。它们没有能量系统,不能自己合成任何物质,也无法主动移动和交流,只能“被动等待”机遇。一旦进入合适的宿主细胞,病毒便会启动复制程序,实现种群的爆发增长。因此,病毒被称为“生命的极简版本”,它舍弃一切冗余,只追求遗传信息的最大化传递效率。
病毒的“极简主义”其实是一种高度进化的策略。通过寄生在宿主身上,病毒不仅大幅降低了自身维持生命活动的能量消耗,还可以快速迭代、适应环境。这种方式让病毒成为地球上种类最多、分布最广的“生物体”之一。
病毒与我们的生活
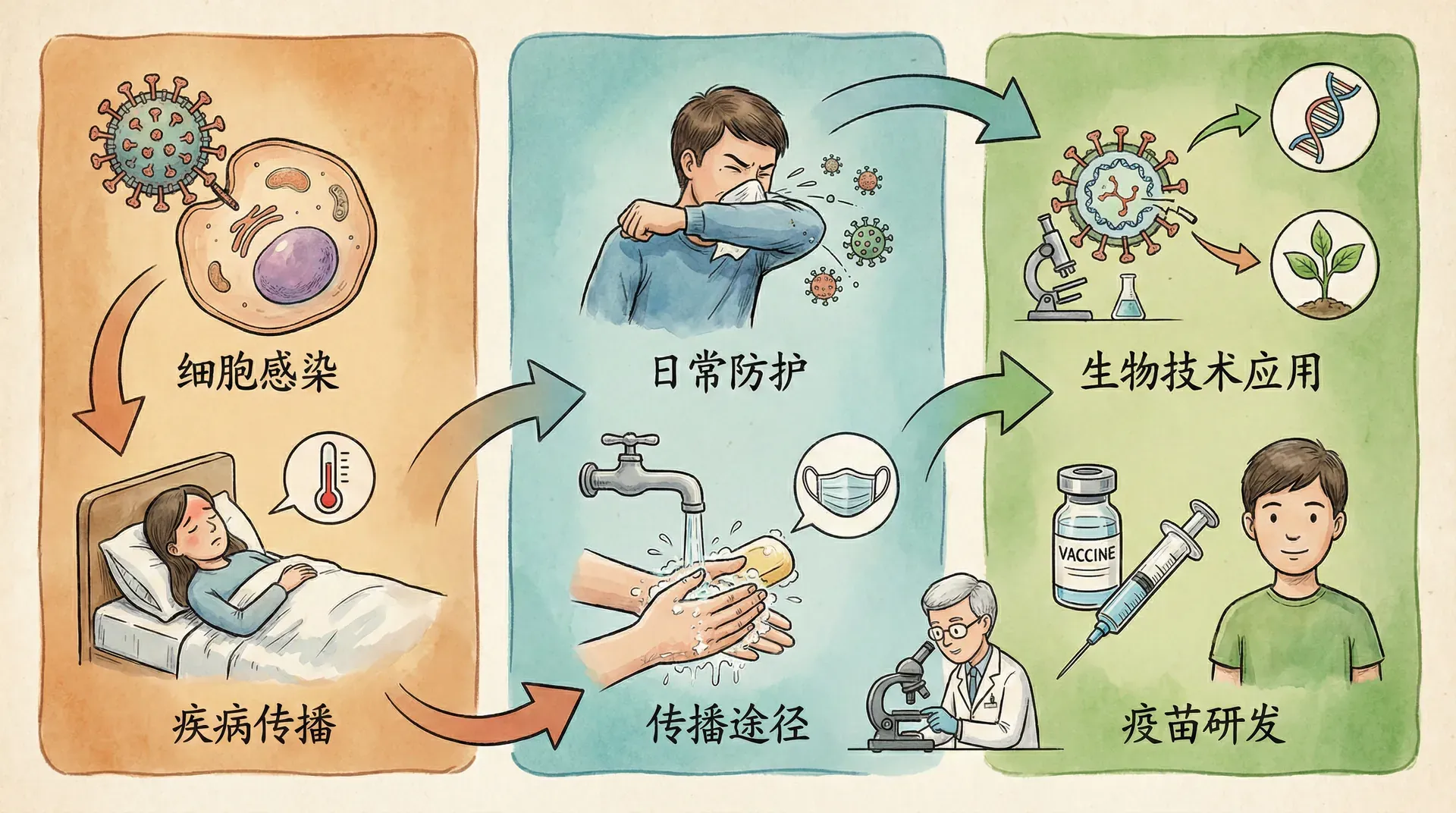
中国常见的病毒疾病
病毒不仅仅是实验室里的“陌生名词”,它们与我们的日常生活息息相关——影响人类健康、农业生产甚至社会运行。中国的病毒性疾病五花八门,每个人都或多或少有相关的生活体验。下面用一个表格梳理部分常见病毒性疾病:
例如,新冠疫情自2020年以来从武汉迅速蔓延到全国;得益于防控和疫苗,社会逐渐恢复秩序。流感是中国人季节性的“老熟人”——北方12月至次年2月南北轮番高发,对儿童、老年人和慢病人群威胁尤大。手足口病则是宝宝群体的“流行病”,每年春夏反复在幼儿园、小学爆发;家长要特别注意孩子卫生和发热症状。乙肝在中国长期是公共卫生关注重点,乙肝疫苗纳入新生儿免疫,成效显著。
此外,轮状病毒肠炎、甲型肝炎、水痘、流行性腮腺炎等也时有出现。有些病毒疾病对农业影响巨大,例如番茄黄化曲叶病毒、小麦条锈病毒等,会导致粮食减产。
病毒如何传播和感染
病毒可谓“伪装高手”,能借助空气、水、动物甚至物品完成跨越式传播。最常见的传播方式有:
可以用下表查阅部分重要传播途径和典型病毒:
实际生活中,一些病毒甚至能组合多种传播方式,以求更高效地扩散。
举个现实案例:2023年冬季,某小学班级手足口病高发,一名学生因口腔疱疹请假,随后全班多名同学出现类似发热、皮疹。经调查,原来大多数孩子在课间热衷于共用玩具,且洗手习惯不到位,导致病毒在人与人之间迅速“接力”。
而在农村,则有稻田条纹叶枯病毒经由水稻灰飞虱传播,一年可在田野间多次循环,把水稻危害推向高峰。
防控措施和个人防护
面对花样繁多的病毒,人类并非束手无策,而是已经形成了科学高效的防控体系——从疫苗到卫生习惯、从消毒措施到环境治理,环环相扣。
疫苗接种——最强“防火墙”
疫苗相当于给人体装上了“人工预警器”,让免疫系统提前识别和清除特定病毒。中国疫苗研发和推广位居全球领先。几项代表性疫苗举例如下:
中国在疫苗研发和生产领域持续走在世界前沿。截至2023年,中国已有多款新冠疫苗获得世界卫生组织紧急使用授权,不仅助力国内疫情防控,还为全球抗击新冠贡献了智慧和力量。
日常生活中的自我防护
- 佩戴口罩:在人多场所和疫情期间减少吸入病毒。
- 勤洗手:肥皂流水最有效,尤其饭前便后、外出归来。
- 开窗通风:减少病毒在空气中的积聚。
- 健康饮食和锻炼:增强免疫力,提高对病毒的抵抗能力。
- 保持社交距离:减少传染机会,尤其是在流行季节或暴发期间。
在人流密集的公共场所,如电梯、地铁、商场等,佩戴口罩,并尽量避免用手直接接触物体表面,这是非常实用且有效的自我防护措施。在幼儿园、学校等高风险区域,日常加强环境消毒及对学生健康状况的监测,也能够极大程度地降低病毒爆发的风险。
总之,疫苗接种、科学防护与环境管理多管齐下,筑起了“抗病毒壁垒”。我们每个人都是守护健康的一员,只要行动得当,病毒并不可怕,健康生活触手可及。
病毒的“生存策略”
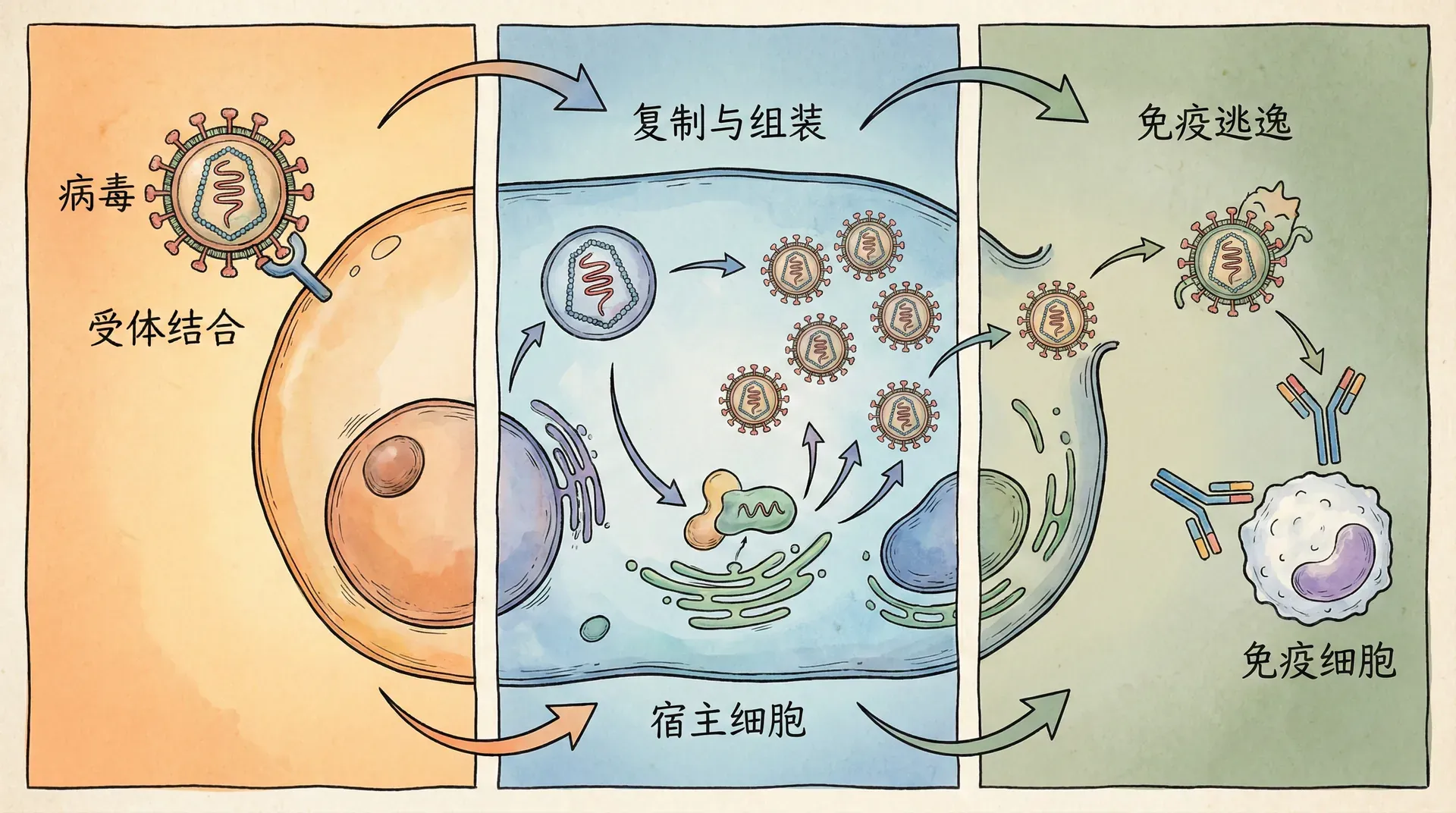
病毒如何“劫持”细胞
病毒的生存策略可以用一个词来概括:寄生。不过,这种寄生远比大多数人想象的要复杂和高明。它们不像跳蚤、寄生虫那样只是“住进”宿主体内,而是像潜伏的“黑客”,精准而隐蔽地接管整个宿主细胞的“操作系统”。病毒几乎没有自己的代谢系统,必须依赖宿主细胞的一切资源生存和复制,这种极致的依赖让病毒成为地球上最“极简主义”的生命形式。
让我们看看这场“生命黑客大战”如何展开。首先,病毒游走在宿主体内,寻找可以感染的目标细胞。可是,细胞并不会轻易敞开大门。只有当病毒表面的特定蛋白质与细胞表面的特定受体“钥匙对锁”时,病毒才能获得进入许可。不同病毒偏爱的“门禁卡”不同,这也解释了为什么某些病毒只感染某一类细胞,比如乙肝病毒主要攻击肝细胞,新冠病毒则偏爱人的呼吸道和肺泡细胞。
当病毒成功“入侵”细胞后,真正的劫持才刚刚开始。它们会将自身的遗传物质(DNA或RNA)注入细胞内部,这些遗传信息立刻“入驻”细胞的各种合成工厂。原本用来保证细胞生长和功能的蛋白合成体系、DNA复制体系,此刻全部被病毒强行“征用”。可以想象,一家本来生产有用器械的工厂,图纸无声无息被偷换,流水线开始大批量制造病毒“零件”。经过组装,一批批新生病毒颗粒伺机而动。
上图展示了病毒在细胞内复制的指数级增长。初期阶段,病毒粒子很少,但当合成工厂按下全力“生产键”,病毒数量会在很短时间内达到成千上万,远超人的直观想象。这也是为什么很多病毒性感染起病时很轻微,可症状却会突然在短时间内恶化——背后就是病毒的爆发式复制。
病毒复制的基本过程
不同种类的病毒复制流程有所区别,但核心步骤惊人地相似,像一条高效的“生产线”。
进厂入门:首先,病毒粒子需要识别并结合细胞表面的适配受体。没有匹配的“门禁码”,病毒寸步难行,这也是宿主特异性的分子基础。例如艾滋病毒要进入T细胞,必须识别CD4受体。
解包卸货:病毒与细胞膜融合后,病毒衣壳解体,释放其遗传物质(DNA或RNA)至细胞内部。有的病毒还需进入细胞核,有的则直接在细胞质开始“工作”。
控制工厂:病毒基因将细胞的合成系统据为己用,指挥蛋白质合成机器批量生产病毒特有的蛋白质及复制病毒自身的核酸。这一环节常配有多种欺骗手段,使宿主无法轻易察觉入侵。
许多病毒还能长期潜伏于宿主细胞,比如疱疹病毒能隐藏在神经细胞多年,一旦人体免疫力下降便“死灰复燃”。这种“潜伏-激活”的生命周期进一步增强了病毒的生存韧性。
不同类型病毒的特点
虽然所有病毒都实行寄生,但不同种类的病毒根据其遗传物质的构造和复制策略,有着本质区别。最主要的分法是DNA病毒和RNA病毒:
DNA病毒像使用“正版软件”的老用户,遗传物质构造严谨、相对稳定,突变率低,因此人类利用疫苗防控这类病毒往往可以取得长期效果,例如乙肝疫苗和水痘疫苗能维持多年免疫力。RNA病毒则相反,它们复制时容易出错,基因突变频繁,也正是因此,像流感、新冠等RNA病毒容易产生变异株,造成疫苗更新频率高、防控难度大。例如每年需要更新的流感疫苗,就是为了应对RNA病毒的快速变异。逆转录病毒最为“阴险”,不仅能将自己的基因整合到宿主染色体内,还能长期潜伏,给治疗带来更大挑战。
这种差异直接影响人类制定防控策略。对稳定型病毒,我们可以集中研发一次性疫苗;对易变异病毒,则需监测变异趋势、快速反应、动态调整疫苗配方。
RNA病毒的高突变率,正是它们潜藏极大危险性的根本原因。一方面,变异带来“伪装能力”,能让它们逃避免疫系统的追捕甚至产生药物耐受性;另一方面,如果突变太多也可能令其“自毁前程”,丧失原有的感染力。在自然界,这是一场病毒与宿主间的进化“军备竞赛”。
人类与病毒的较量
疫苗的防护原理
疫苗是人类对抗病毒最重要的武器之一。疫苗的工作机制,并非直接杀灭病毒,而是激活人体免疫系统的“记忆力”,提前让身体识别并储存对某种病毒的免疫响应。当真正的病毒来袭时,免疫大军已整装待发,可第一时间发现并清除病毒。
传统疫苗方法,包括“灭活疫苗”和“减毒活疫苗”。灭活疫苗类似用病毒的“标本”做演习,虽然病毒已失活,但仍可展示其外形抗原,让免疫系统识别和记住。减毒活疫苗则采用弱化后的病毒,刺激免疫系统产生更持久的免疫力。例如小儿麻痹疫苗、麻疹疫苗等。
近年来的科技突破,特别是mRNA疫苗,把疫苗技术推到了新高度。mRNA疫苗好比给人体细胞递交一份“虚拟病毒说明书”,让细胞短暂地合成病毒的某个无害蛋白,诱导免疫系统识别。这样可以显著提升生产速度与安全性。例如新冠mRNA疫苗的问世,大大加快了疫情防控步伐。中国多家企业也在推动mRNA疫苗创新,进入全球前沿行列。
抗病毒药物的作用机制
若感染已发生,抗病毒药物成为极其关键的生命线。理论上,“杀病毒”并不像“杀细菌”那样容易,因为病毒藏身在宿主细胞里,过度杀伤等于牺牲自身细胞。因此,理想的抗病毒药物,要能“精准打击”病毒的关键环节,让病毒自动“瘫痪”在复制线上。
主要抗病毒药物有三大类:
此外,近年来还出现能阻断病毒与细胞受体结合的“融合抑制剂”、影响病毒外壳稳定的分子等创新药物。
新冠疫情期间,中医药疗法(如连花清瘟、金花清感等)也进入科学验证阶段,展示出一定的抗病毒效果。这说明多路径、跨学科治疗思路正成为抗病毒领域的新趋势。
要研发一种新药,从分子设计、实验、动物和临床试验到最终上市,通常历时10-15年,耗费数十亿美元。新冠疫情启动了空前的全球合作,使很多候选药物和潜在疗法进入“快车道”,但基础研究和安全性评估依然不可省略。
未来的挑战与希望
病毒的世界远比人类复杂。每年都有新型病毒出现,如埃博拉、寨卡、冠状病毒等不断挑战科学家极限。未来抗病毒领域面临诸多挑战,但也充满希望:
-
快速变异,适应力强:RNA病毒尤其如此,新冠的Omicron变异株就是典型。人类迫切需要建立可以“定制更新”的快速疫苗平台,及时响应病毒的进化。
-
抗药性风险:抗生素滥用已招致细菌耐药,抗病毒药物如不慎用也会加速耐药株出现。只有多靶点、组合治疗、精准医学才能持续应对。
-
全球流动性带来新风险:人口流动加速,病毒传播周期变短,疫情“跨境”概率大增。这呼吁全球协作,科学预警,公共卫生系统需不断升级。
-
新技术带来的机遇:人工智能正在革新药物筛选,帮助科研人员更快找到病毒的“生命弱点”;基因编辑手段如CRISPR,可以精准“剪切”病毒基因,有望带来颠覆性疗法;结构生物学助力病毒成分三维解析,为未来“定制药物”提供数据基础。
近年来全球疫苗研发投入快速增长,特别是在新冠疫情的推动下,2020年后研究投入进入“爆发期”。这不仅极大提升了抗病毒能力,也反过来促动了癌症、罕见病等疫苗创新速度。
中国在这场人类与病毒的较量中扮演着越来越重要的角色。不仅在新冠疫苗、抗病毒药物的研发生产上走在世界前列,传统中医药现代化、中西医结合体系也吸引全球关注。中国科学家持续在病毒溯源、新型疫苗、基因编辑等前沿领域发力。同时,中国积极参与全球疫情援助、疫苗共享,践行“人类卫生健康共同体”理念。
病毒虽小,却推动地球生物进化史向前滚动,更在无数疫情危机中打磨人类的智慧、勇气与团结。当我们了解病毒的本质和生存规律,也许就能更有把握地守护健康、创造更安全的社会。在这场持续数千年的博弈中,科学和知识终将成为人类最强大的武器,持续引领我们迎接未知的病毒挑战。