无细胞生物系统
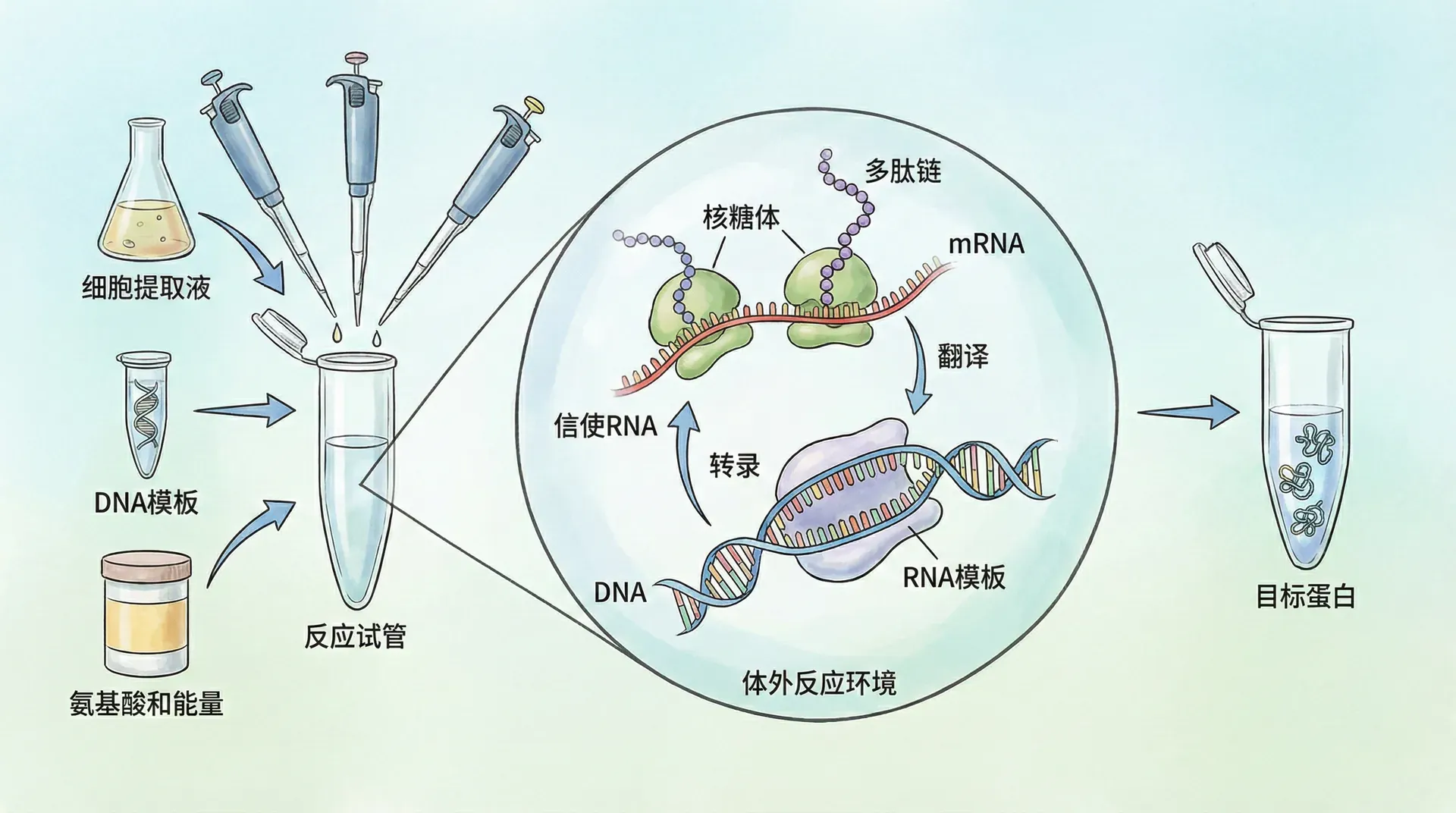
现代社会对绿色与可持续生产的需求不断提升,推动生物制造技术向更高效、安全、环保的方向发展。以往依赖微生物发酵,通过培育细胞来合成各类目标产物,但受到细胞自身复杂代谢和耐受能力的制约,传统发酵在调控、产物纯度和提升效率方面存在明显局限。
为突破这些瓶颈,无细胞生物系统应运而生,并成为生物制造的新兴焦点。通过提取细胞内的核心功能组分(如酶和辅因子等),在体外搭建高效的人工生物反应体系,无需依赖活细胞,实现更加灵活和精准的反应设计,有效提升了产率和适应性。
无细胞生物系统是在体外环境下利用酶等生物分子重建并驱动特定生化反应或产物合成的技术平台,无需完整活细胞参与。常见类型包括粗酶反应体系、纯化酶级联和无细胞蛋白合成系统等。
可以将无细胞系统比作搭建乐高积木:根据需求灵活选择、组合不同的功能模块,组装出专属生产线,而无需维护一整个复杂的“生物工厂”。这一理念带来更高的操作自由度和反应效率。与此同时,无细胞系统还具有高度可编程性,便于快速尝试新型反应路径,广泛应用于新药开发、化学品合成等领域。
技术发展历程
历史回顾
生物制造技术的发展历程可以追溯到数千年前。我国古代就已利用微生物进行酿酒、制醋、发酵豆制品等食品制造,形成了丰富的生物制造经验。19世纪中后期,路易·巴斯德通过实验证明了酵母细胞在酒精发酵中的决定性作用,推动了微生物学和现代生物技术的起步。值得一提的是,1897年德国科学家布赫纳首次实现了无细胞原料发酵(酵母细胞提取液发酵葡萄糖生成乙醇),不仅展示了细胞成分体外催化反应的可能性,还为酶学和代谢工程奠定了理论基础。布赫纳也因此获得了1907年诺贝尔化学奖。
自20世纪以来,随着生物化学、分子生物学和工程技术的发展,无细胞技术从最初的基础发现逐步演变为可产业化应用的平台。例如,20世纪70年代酶固定化技术大大提高了工业反应的稳定性和可控性;1999年基于纯化因子组装的无细胞蛋白合成系统(PURE system)诞生,推动了高通量蛋白合成、蛋白药物开发和合成生物学研究。近年来,自动化、高通量、模块化设计等新兴手段也加速了无细胞系统的工程化进程。
近年来,中国在无细胞生物系统的理论研究和技术产业化方面均取得了令人瞩目的进步。中科院、清华大学、华东理工大学等顶尖科研院所以及多家重点实验室,积极开发无细胞催化、合成途径优化、系统组装等前沿领域,在核心酶制备、反应系统优化、自动化集成等关键技术节点取得突破。
华大基因、百济神州、药明康德等生物技术企业也逐步将无细胞系统用于药物发现、疫苗研制、医药中间体等实际生产之中。一些企业还布局无细胞蛋白合成服务、工艺自动化平台等新兴赛道,不断推动我国无细胞生物制造的创新与产业化能力走在国际前列。
核心工作原理
系统分类对比
无细胞生物系统与传统微生物发酵系统最大的本质区别在于是否需要完整的活细胞参与反应。在传统发酵系统中,微生物细胞承担了原料转化、催化反应、能量代谢等全部功能,但细胞自身的复杂调控容易带来副产物生成、反应最优条件受限、耐毒性低等问题。与此相对,无细胞系统舍弃了细胞壁、细胞膜等生理障碍,直接利用纯化酶或粗提物在体外完成精细化反应,可实现更高效率、更高产物纯度与灵活的反应设计。
技术分类
按照系统设计的复杂程度与应用范围,无细胞生物系统可分为以下四种主要类型,每种类型在酶的数量、工程难度和应用场景上各具特色:
- 单酶系统:仅使用一种关键酶催化反应,操作简单,适用于高专一性生物转化,如单一步骤的底物-产物转换(如葡萄糖氧化酶检测葡萄糖)。
- 多酶反应系统:多种酶协同工作,形成级联反应,实现复杂化合物的高效合成,常用于精细化学品、合成中间体等场景。
- 无细胞发酵(cell-free fermentation):模拟完整的细胞代谢途径,保留关键能量与物质合成模块,能够持续产出复杂分子(如无细胞合成氨基酸、脂肪酸等)。
- 全细胞发酵:作为对照,此类别仍涉及完整活细胞的传统生物制造过程,系统极为复杂,调控难度大,但工业基础成熟。
主要技术优势
反应速度更快
传统微生物系统受到细胞膜的限制,物质传递速度较慢。无细胞系统没有这种障碍,可以实现更快的反应速度。这就像是高速公路与城市道路的区别,没有了红绿灯和拥堵,车辆可以更快到达目的地。
更快的反应速度不仅意味着更短的生产周期,也为连续化工业生产和应急生物制造提供了基础。在一些高附加值反应和应急疫苗生产中,无细胞系统能够在数小时内响应突发需求,极大提高了生物制造的灵活性和时效性。
提高有毒物质耐受性
许多工业生产过程会产生对细胞有害的副产物。以丁醇生产为例,传统微生物在丁醇浓度达到1%时就会因为细胞膜受损而停止生产,但无细胞系统可以在4%的丁醇浓度下正常工作。
与活细胞不同,无细胞系统缺少生物膜等脆弱结构,因此可以在高浓度底物、高盐度/有机溶剂等极端条件下稳定运行。这一特性适用于生产多种有毒、难降解或强氧化等特殊环境下的化学品,也方便了底物浓缩和产物分离工艺的设计,提高了整体经济性。
实现非天然反应
无细胞系统可以组合细胞内外的酶类,实现自然界中不存在的生化反应。比如将纤维素直接转化为淀粉,这在自然界中是不可能发生的过程。
这种"拆解重组"的能力使得无细胞系统能够跨越自然界的限制,创造出全新的生物合成途径。
由于无细胞系统可以灵活地选择任意来源的酶进行模块化组装,科学家能够自由设计和拼接路径,不受生物体固有代谢网络的限制。除了“纤维素到淀粉”这样的突破性反应,还可以构建“化学定制”生产流程,实现精细化新材料、超长链脂肪酸、医药前体等高难度合成。
系统高度可控和可编程
无细胞平台的各类反应参数(如酶浓度、底物配比、pH、温度)均可单独或联动高精度调控。通过自动化/数字化工具,能够实现实验流程标准化和高通量筛选,显著提升研发效率。此外,反应无需活体生长周期,无需考虑细胞增殖、自噬等复杂调控,极易实现对产率、选择性等核心指标的按需优化。
主要应用领域
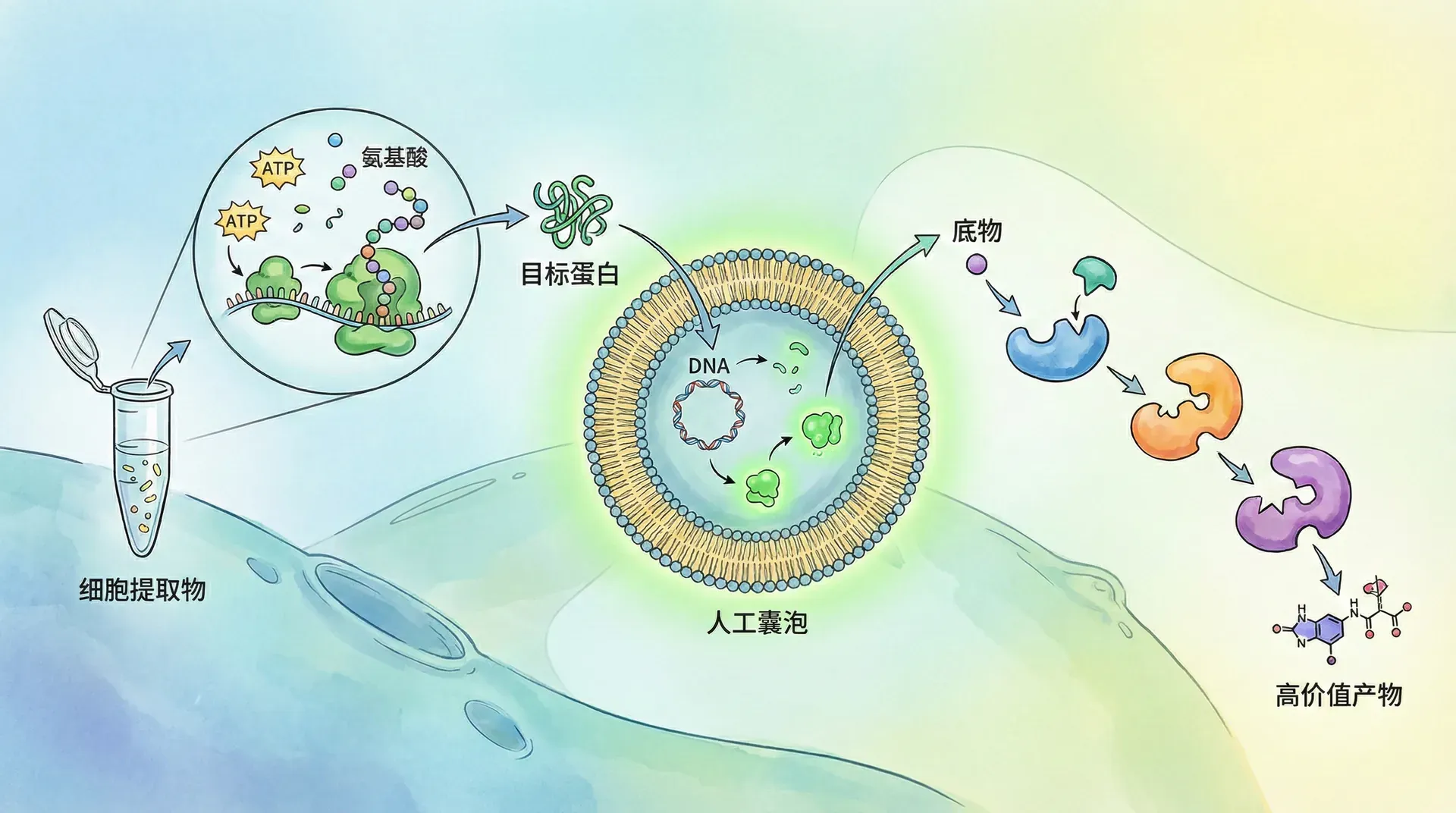
无细胞生物系统目前正广泛应用于多个前沿与工业领域,主要有三大应用方向:
无细胞蛋白质合成
传统蛋白质生产依赖大肠杆菌、酵母等微生物宿主,但这些系统存在包涵体形成、蛋白酶降解、毒性蛋白表达受阻以及同位素/非天然氨基酸掺入效率低等问题。无细胞蛋白质合成系统能够精准控制反应环境,实现高效、可控、高通量的蛋白生产。
无细胞系统可以实现多重蛋白质快速表达、自动化蛋白质组装、靶向修饰等新功能,同时还能表达各类不稳定、低丰度或对宿主毒性的蛋白分子。近年来,华大基因等中国生物技术公司已经开始利用无细胞蛋白合成技术生产诊断试剂和疫苗组分,在分子诊断和抗原开发等领域表现突出。高通量无细胞蛋白合成还大幅提升了蛋白药物研发、抗体筛选、酶工程等关键领域的创新速度。
体外合成生物学
体外合成生物学是设计和构建人工生物系统的新兴领域。相比于改造活细胞,在体外构建生物系统更加灵活和可控。
除基本合成反应外,体外平台还支持对复杂代谢途径的迭代优化、大规模文库筛选以及新型功能模块(比如合成辅酶、光合模块)的自由集成。这极大地加速了新型催化循环、人工代谢网络的构建。
中科院在2023年成功构建了一个包含30多种酶的人工光合作用系统,实现了二氧化碳到淀粉的高效转化,这项技术有望为解决粮食安全问题提供新方案。
此外,体外合成生物学为基础科学探索打开了新路径,例如人工生命起源实验、合成极简细胞等,是合成生物学与材料科学、能源科学交叉创新的重要平台。
合成酶途径生物转化
将无细胞技术应用于大宗化学品生产是当前最具工业潜力的方向。与传统发酵相比,无细胞途径能够跳过“维持生命”耗能,最大限度地推进底物到产物的高转化率。此外,由于无细胞平台对反应组分无严格来源限制,能够拼接跨物种、跨域的酶体系,实现原料调换和产品定制,极大丰富了可生产分子的谱系。
将这一能力应用到高值医药中间体、精细化学品和大宗能源材料等领域,有望实现小体积高效率工厂、灵活定制生产体系,对能源、医药、材料等传统产业带来深刻变革。
生物燃料生产
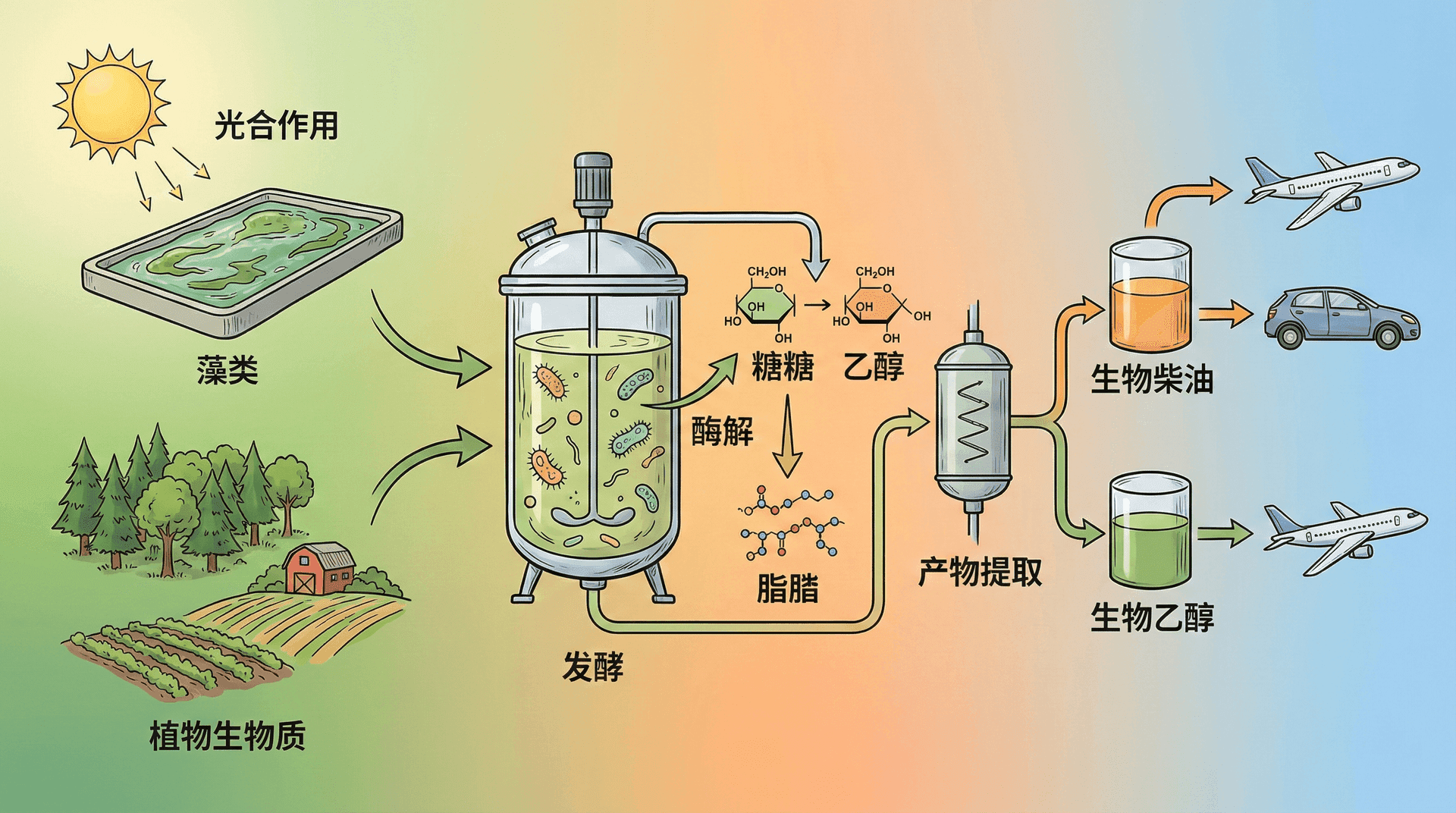
氢气制备
氢气作为清洁能源载体,在中国的能源转型中扮演着日益重要的角色。然而,传统制氢方法(如化石燃料裂解、水电解)不仅能耗高,还会带来严重的二氧化碳和有毒副产物排放。无细胞生物制氢系统通过设计高效合成酶途径,可以从玉米淀粉、秸秆等农业废料中直接高效产氢,过程绿色环保。
该系统包含四个关键步骤的酶反应,理论上每分子葡萄糖可以产生12分子氢气,几乎接近化学极限。中科院大连化物所在相关技术方面取得了重要进展,实现了底物高转化率与副产物极低的良好结合。在未来分布式能源、工业制氢等场景中,无细胞产氢路线有望成为可持续氢能产业链的关键技术之一。
生物乙醇和丁醇
无细胞系统生产酒精具有显著优势。通过添加ATP酶或使用砷酸盐替代磷酸盐,可以突破传统细胞代谢对ATP平衡的限制,使葡萄糖到乙醇的转化率达到99%。这意味着180克葡萄糖可以产生90克乙醇,反应在8小时内完成。
除了高收率和快速生产,无细胞酒精合成还可以大幅减少副产物的产生,降低产物分离和纯化成本。在绿色酒精和有机溶剂等领域,展现出比传统发酵更优的能源利用效率和工业适应性。
生物电力系统
酶燃料电池是一种利用酶催化将化学能直接转化为电能的创新装置。与传统微生物燃料电池相比,酶燃料电池没有细胞膜的阻隔,可以实现更高的功率密度和更简化的系统设计。
酶燃料电池不仅可以利用各种生物基有机物发电,还因其绿色、温和反应条件,成为下一代便携式医疗器械和低能耗电子设备的理想能量解决方案。
目前酶燃料电池还面临酶稳定性差、功率输出低等挑战,但随着酶工程与固定化技术的发展,这些问题正在逐步解决。
中科院的研究团队通过固定化技术,成功将11种酶组装在碳电极表面,模拟完整的柠檬酸循环,实现了糖类到电能的直接转化。未来,随着材料工程和酶改造技术的进步,有望构建高效、稳定、可规模化生产的新型生物发电系统,为绿色能源革命提供坚实技术基础。
技术挑战与发展前景
随着无细胞生物系统技术的飞速发展,其在现代生物制造中的应用边界不断被拓展。然而,要实现从实验室到大规模产业化,无细胞系统仍需突破多方面的技术壁垒。深入理解这些挑战,并积极探索前沿解决方案,是推动该领域健康可持续发展的关键。
主要技术瓶颈
无细胞生物系统要想实现真正的大规模产业化应用,还需要跨越以下几大技术鸿沟:
此外,底物来源的多样性、产物分离提纯的便捷性、系统在动态环境下的稳健性等也是亟需关注的方向。只有上述多个关键环节联动突破,无细胞系统才能高效、安全、经济地服务于真实产业。
中国的发展机遇
中国在无细胞生物系统领域同样站在全球科技创新的前沿,面临着难得的历史性发展机遇:
预计到2030年,无细胞生物系统将在高值医药、特色化学品、生物能源等细分领域率先实现产业化,成为中国生物制造创新的重要发动机和战略支撑,为实现“双碳”目标、推动高质量发展注入新动能。
总结
无细胞生物系统是指在体外直接利用酶等生物组分,开展高度可控的生化反应,这一方式突破了传统细胞的边界,展现出独特的优势。与传统体系相比,无细胞系统的催化反应不仅可以灵活编程和高速进行,还拥有更强的对有毒底物及产物的耐受性,能够实现许多天然细胞无法胜任的新型反应路线。
目前,无细胞生物系统在蛋白质合成、高值化学品生产、绿色能源转化、新药开发以及环境治理等领域展现出了广泛的应用前景,已成为合成生物学不可或缺的重要支撑技术。随着酶工程、工艺优化及自动化技术的不断进步,预计未来十年内,无细胞系统将在多个产业领域实现从实验室到规模化应用的跃迁,助力我国生物制造产业的升级和绿色发展。
总体来看,无细胞生物系统不仅代表了现代生物制造的新范式,也为解决能源短缺、环境污染、健康挑战等问题提供了具有广阔前景的技术路径。只要产业各方加强协作与持续创新,这一技术将在未来社会经济发展中发挥不可替代的重要作用。