新陈代谢导论
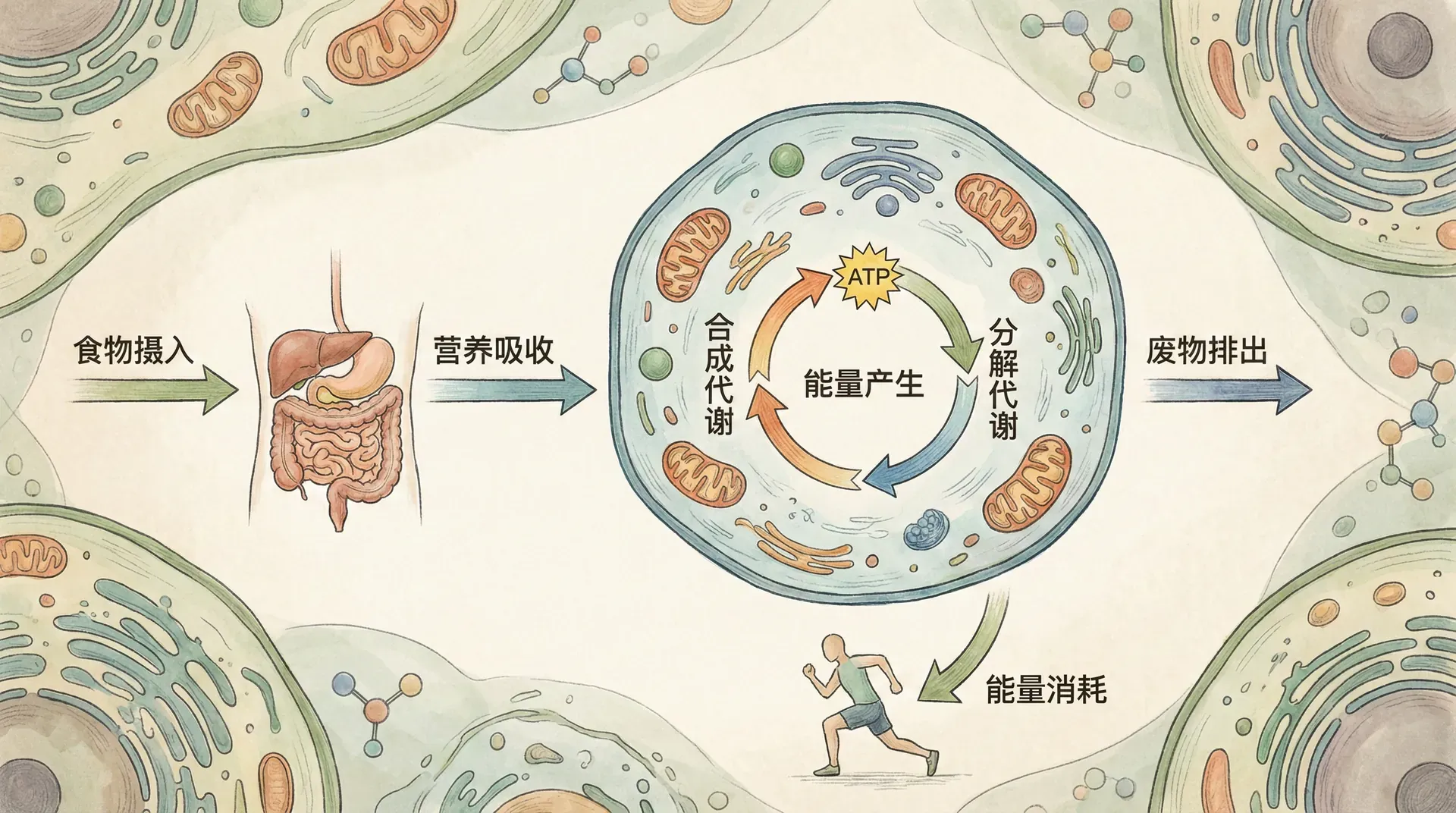
生物细胞犹如一个微型化工厂,在微观空间内进行着数千种化学反应。就像深圳的比亚迪工厂将原材料转化为电动汽车,细胞能够将糖类转化为氨基酸,再将氨基酸组装成蛋白质。当我们消化食物时,蛋白质被分解为氨基酸,这些氨基酸又可以转化为糖类。在多细胞生物中,细胞生产的化学产物常常被运输到生物体的其他部位使用。
细胞呼吸作用是细胞经济运转的驱动力,通过提取糖类和其他燃料中储存的能量来维持各种生命活动,比如物质跨膜运输等细胞工作。
在东海和南海的夜晚,海浪常常闪闪发光,这种现象被称为“海火”。造成这种奇观的是一种叫做甲藻的单细胞海洋生物。甲藻能够将储存在有机分子中的能量转化为光能,这个过程叫做生物发光。大多数发光生物生活在海洋中,不过陆地上也有,比如夏夜里常见的萤火虫。
生物发光和其他代谢活动都受到精确的协调和控制。细胞在复杂性、效率和对微妙变化的反应能力方面,是无与伦比的化学工厂。我们接下来学习的新陈代谢概念将帮助理解物质和能量如何在生命过程中流动,以及这种流动如何被调节。
生物体的新陈代谢
生物体所有化学反应的总和称为新陈代谢。新陈代谢是生命的突现性质,源于分子间有序的相互作用。
代谢途径的组织结构
我们可以将细胞的新陈代谢想象成一张复杂的道路网,包含数千种化学反应,排列成相互交叉的代谢途径。一条代谢途径从特定分子开始,经过一系列限定的步骤,产生特定的产物。途径中的每一步都由特定的酶催化:
调节这些酶的机制平衡着代谢的供给和需求,就像城市交通信号系统中的红、黄、绿灯控制车流一样。
新陈代谢管理着细胞的物质和能量资源。一些代谢途径通过分解复杂分子为简单化合物来释放能量,这些降解过程称为分解代谢途径。分解代谢的主要途径是细胞呼吸,其中葡萄糖和其他有机燃料在氧气存在下被分解为二氧化碳和水。
与之相对,合成代谢途径消耗能量来从简单分子构建复杂分子,有时称为生物合成途径。合成代谢的例子包括从简单分子合成氨基酸,以及从氨基酸合成蛋白质。
分解代谢和合成代谢是代谢景观中的“下坡”和“上坡”路径。分解代谢“下坡”反应释放的能量可以储存起来,然后用于驱动合成代谢的“上坡”反应。
能量转换定律
研究物质集合中发生的能量转换的学科称为热力学。科学家用“系统”一词表示所研究的物质,用“环境”指系统外的宇宙其余部分。
生物体是开放系统。它们吸收能量(例如光能或有机分子形式的化学能),并向环境释放热量和代谢废物,如二氧化碳。
热力学第一定律
根据热力学第一定律,宇宙的能量是恒定的:能量可以转移和转换,但不能创造或销毁。第一定律也被称为能量守恒定律。
就像国家电网不制造能量,只是将能量转换为便于我们使用的形式。植物通过将阳光转化为化学能,充当能量转换器,而不是能量生产者。
例如,大熊猫将食物中有机分子的化学能转换为动能和其他形式的能量来进行生物活动。这些能量在执行工作后会发生什么?热力学第二定律帮助我们回答这个问题。
热力学第二定律
如果能量不能被销毁,为什么生物体不能简单地循环利用它们的能量?事实上,在每次能量转移或转换中,一些能量变得不可用于做功。在大多数能量转换中,可用形式的能量至少部分转换为热能并以热的形式释放。
在进行各种工作的化学反应过程中,活细胞不可避免地将其他形式的能量转换为热。系统只有在存在温度差异,导致热能从较热位置流向较冷位置时,才能利用这种能量做功。如果温度均匀(如在活细胞中),化学反应产生的热量只会加热物质,比如使生物体升温。
失去可用能量作为热量释放到环境中的结果是,每次能量转移或转换都使宇宙变得更加无序。科学家用熵来衡量分子无序或随机性。物质排列越随机,其熵越大。
现在我们可以陈述热力学第二定律:每次能量转移或转换都增加宇宙的熵。虽然局部有序可以增加,但整个宇宙有着不可阻挡的随机化趋势。
生物有序与无序
生物系统增加其环境的熵,正如热力学定律所预测的。细胞确实从较少组织化的起始材料创造有序结构。例如,简单分子被组织成氨基酸的更复杂结构,氨基酸被组织成多肽链。
生物体在进化过程中复杂性增加并不违反第二定律。特定系统(如生物体)的熵实际上可以减少,只要宇宙总熵(系统加环境)增加。因此,生物体是日益随机的宇宙中的低熵岛屿。
自由能变化
热力学定律适用于整个宇宙。作为生物学家,我们想了解生命的化学反应——例如,哪些反应自发发生,哪些需要来自外部的能量输入。
自由能变化 ΔG
1878年,耶鲁大学的吉布斯教授定义了一个非常有用的函数,称为系统的吉布斯自由能(不考虑其环境),用字母G表示。自由能是系统能量中在温度和压力均匀的情况下(如在活细胞中)能够做功的部分。
自由能变化ΔG可以用以下方程计算:
其中:
- ΔH表示系统焓的变化(在生物系统中等同于总能量)
- ΔS是系统熵的变化
- T是绝对温度(开尔文单位)
只有ΔG为负值的过程才是自发的。换句话说,每个自发过程都减少系统的自由能,而ΔG为正值或零的过程永远不会自发进行。
放能反应和吸能反应
基于自由能变化,化学反应可以分为放能("能量向外")或吸能("能量向内")。放能反应伴随净自由能释放进行,因为化学混合物失去自由能(G减少),所以放能反应的ΔG为负值。
我们可以用细胞呼吸的总反应作为例子:
在标准条件下,每摩尔(180g)葡萄糖被呼吸分解,有686千卡(2870千焦)的能量可用于做功。
吸能反应从环境中吸收自由能。因为这种反应实质上在分子中储存自由能(G增加),所以ΔG为正值。这种反应是非自发的,ΔG的大小就是驱动反应所需的能量。
新陈代谢与平衡
孤立系统中的反应最终会达到平衡,然后就不能做功了。新陈代谢的化学反应是可逆的,如果在试管的孤立环境中进行,它们也会达到平衡。因为平衡系统处于G的最小值且不能做功,达到代谢平衡的细胞是死亡的! 新陈代谢作为整体永远不处于平衡状态,这是生命的定义特征之一。
ATP
细胞进行三种主要工作:化学工作(推动不会自发发生的吸能反应)、运输工作(将物质逆着自发运动方向泵送跨膜)、机械工作(如纤毛摆动、肌肉细胞收缩)。
细胞管理能量资源来完成这些工作的关键特征是能量偶联,即利用放能过程驱动吸能过程。ATP负责介导细胞中的大多数能量偶联,在大多数情况下作为为细胞工作提供能量的直接来源。
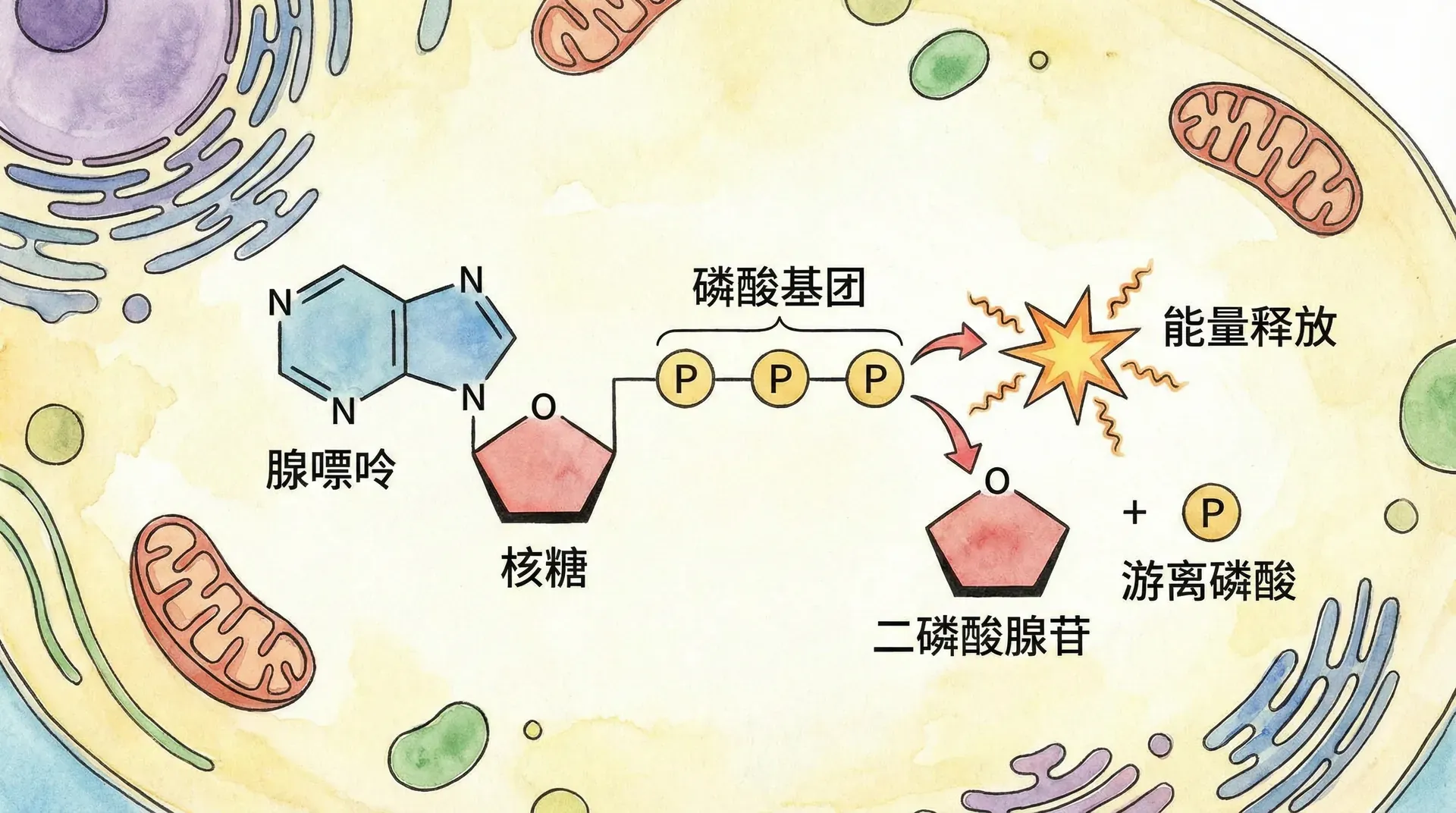
ATP的结构和水解
ATP(三磷酸腺苷)含有糖类核糖,连接着含氮碱基腺嘌呤和由三个磷酸基团组成的三磷酸基团。
ATP磷酸基团之间的键可以通过水解断裂。当末端磷酸键被水分子加成断裂时,一个无机磷酸分子离开ATP,ATP变成二磷酸腺苷或ADP。该反应是放能的,每摩尔ATP水解释放7.3千卡能量:
ATP水解如何执行工作
在试管中,ATP水解释放的自由能仅仅加热周围的水。在生物体中,这种产热有时是有益的。例如,颤抖过程利用肌肉收缩中的ATP水解来温暖身体。
然而,细胞的蛋白质以几种方式利用ATP水解释放的能量来执行三种类型的细胞工作。细胞能够利用ATP水解释放的能量直接驱动本身是吸能的化学反应。如果吸能反应的ΔG小于ATP水解释放的能量,则两个反应可以偶联,使得总体上偶联反应是放能的。
这通常涉及磷酸化,即将磷酸基团从ATP转移到其他分子(如反应物)。带有共价结合磷酸基团的受体分子称为磷酸化中间体。
运输和机械工作也几乎总是由ATP水解驱动。在这些情况下,ATP水解导致蛋白质形状改变,通常改变其结合另一个分子的能力。
ATP的再生
生物体连续使用ATP,但ATP是可以通过向ADP添加磷酸来再生的可再生资源。无机磷酸和能量的这种穿梭称为ATP循环,它将细胞的产能(放能)过程与耗能(吸能)过程偶联。
ATP循环以惊人的速度进行。例如,一个工作中的肌肉细胞在不到一分钟内回收其整个ATP库。这种周转代表每个细胞每秒消耗和再生1000万个ATP分子。
因为可逆过程的两个方向不能都是下坡的,ATP的再生必然是吸能的:
分解代谢(放能)途径,特别是细胞呼吸,为ATP的吸能形成过程提供能量。植物也利用光能产生ATP。
酶降低能垒加速反应
热力学定律告诉我们在给定条件下什么会发生和什么不会发生,但对这些过程的速率却什么都没说。自发化学反应无需外部能量要求就可发生,但可能发生得非常缓慢以至于难以察觉。
活化能屏障
每个化学反应都涉及键的断裂和形成。要达到键能改变的扭曲状态,反应物分子必须从环境中吸收能量。启动反应所需的初始能量投入——扭曲反应物分子使键能断裂所需的能量——称为活化能或EA。
酶如何加速反应
酶是充当催化剂的大分子,能够加速反应而不被反应消耗。没有酶的调节,代谢途径中的化学交通会变得极其拥堵,因为许多化学反应需要很长时间。
酶通过降低EA屏障来催化反应,使反应物分子能够在中等温度下吸收足够能量达到过渡状态。
至关重要的是要注意,酶不能改变反应的ΔG;它不能使吸能反应变成放能反应。酶只能加速本来最终会发生的反应。
酶的底物特异性
酶作用的反应物称为酶的底物。酶与其底物结合,形成酶-底物复合体。当酶和底物结合时,酶的催化作用将底物转换为反应的产物。
大多数酶名称以-ase结尾。例如,蔗糖酶催化双糖蔗糖水解为两个单糖——葡萄糖和果糖。
酶分子的只有一个受限区域实际与底物结合。这个区域称为活性位点,通常是酶表面的一个口袋或凹槽。活性位点通常只由酶的少数几个氨基酸形成,蛋白质分子的其余部分提供决定活性位点形状的框架。
特定量的酶将底物转化为产物的速率部分取决于底物的初始浓度。可利用的底物分子越多,它们越频繁地进入酶分子的活性位点。然而,向固定浓度的酶添加更多底物推动反应的速度是有限的。在某一点,底物浓度足够高,所有酶分子的活性位点都被占据。
局部条件对酶活性的影响
温度和pH是影响酶活性的重要环境因素。直到某一点,酶反应速率随温度升高而增加,部分因为底物与活性位点碰撞更频繁。超过那个温度,酶反应速率急剧下降。
大多数人类酶的最适温度约为35-40°C。每个酶也有一个最适pH值。大多数酶的最适pH值在6-8范围内,但也有例外。
酶抑制剂
某些化学物质选择性地抑制特定酶的作用。一些可逆抑制剂类似于正常底物分子,与底物竞争进入活性位点。这些模拟物称为竞争性抑制剂,通过阻止底物进入活性位点来降低酶的生产力。
相比之下,非竞争性抑制剂不直接与底物竞争结合到活性位点。相反,它们通过结合到酶的另一部分来阻碍酶反应。
酶活性调节
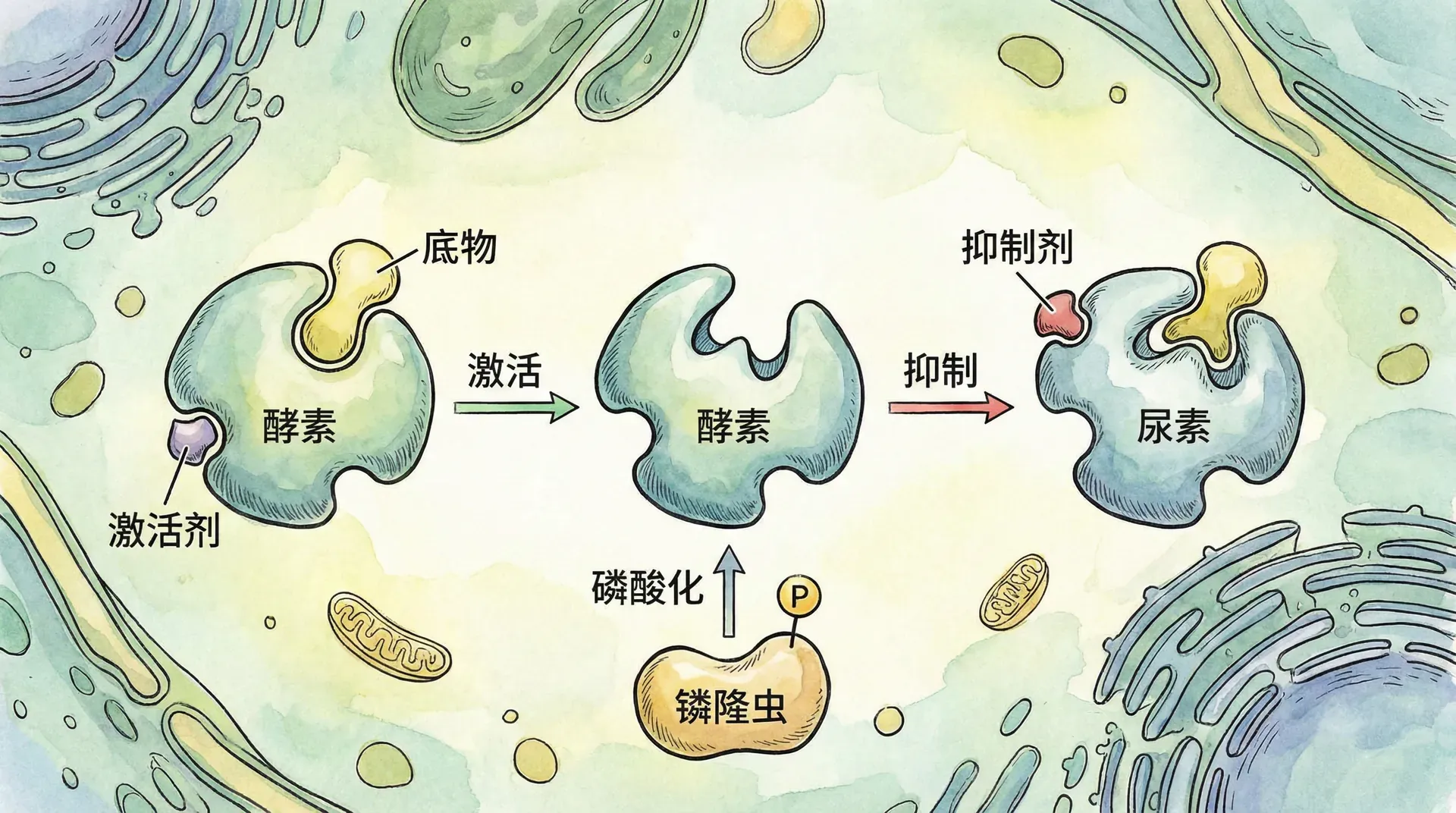
如果细胞的所有代谢途径同时运行,将导致化学混乱。生命过程固有的是细胞严格调节其代谢途径的能力,控制各种酶何时何地活跃。
酶的变构调节
在许多情况下,在细胞中自然调节酶活性的分子表现得像可逆的非竞争性抑制剂:这些调节分子通过结合到分子上的其他位点,改变酶的形状和其活性位点的功能。
变构调节是用来描述蛋白质在某一位点的功能受调节分子结合到独立位点影响的术语。它可能导致酶活性的抑制或刺激。
反馈抑制
我们讨论了ATP生成途径中酶被ATP本身变构抑制。这是代谢控制的常见模式,称为反馈抑制,其中代谢途径被其终产物与途径早期作用的酶的抑制性结合所停止。
一些细胞用这个五步途径从苏氨酸(另一种氨基酸)合成氨基酸异亮氨酸。当异亮氨酸积累时,它通过变构抑制途径第一步的酶来减慢自身合成。因此,反馈抑制防止细胞制造超过必需的异亮氨酸,从而避免浪费化学资源。
细胞内酶的定位
细胞不只是一袋化学物质,其中数千种不同的酶和底物随机混合。细胞是分室化的,细胞结构有助于使代谢途径有序化。
在某些情况下,代谢途径几个步骤的酶团队被组装成多酶复合体。这种排列促进反应序列,第一个酶的产物成为复合体中相邻酶的底物,依此类推,直到释放终产物。
一些酶和酶复合体在细胞内有固定位置,充当特定膜的结构组件。其他酶在特定膜包围的真核细胞器内的溶液中,每个细胞器都有自己的内部化学环境。因此,新陈代谢概念将继续在我们理解生命过程中发挥重要作用,特别是在学习细胞呼吸这一主要分解途径时,它分解有机分子并释放可用于生命关键过程的能量。